题目内容
7.设NA为阿伏加德罗常数的数值,下列说法中正确的是( )| A. | 1 mol Cl2溶于水的过程中有1NA个电子转移 | |
| B. | 100℃时,1L pH=1的硫酸溶液中,含有0.1NA个H+ | |
| C. | 常温常压下,15g HCHO含有1.5NA对共用电子对 | |
| D. | 0.1mol•L-1的醋酸溶液中CH3COO-少于0.1NA个 |
分析 A.氯气与水反应为可逆反应,不能进行到底;
B.100℃时,1L pH=1的硫酸溶液中氢离子浓度为10-1mol/L,依据n=CV计算解答;
C.1个甲醛分子含有4对共用电子对;
D.溶液体积未知.
解答 解:A.氯气溶解于水只有少部分和水反应,Cl2+H2O═HCl+HClO,1mol Cl2溶于水的过程中电子转移小于NA个,故A错误;
B.100℃时,1L pH=1的硫酸溶液中氢离子浓度为10-1mol/L,则1L pH=1的硫酸溶液中,含有氢离子物质的量为0.1mol/L×1L=0.1mol,含有0.1NA个H+,故B正确;
C.常温常压下,15g HCHO物质的量为$\frac{15g}{30g/mol}$=0.5mol,含有对共用电子对0.5mol×4=2mol,2NA对,故C错误;
D.溶液体积未知,无法计算醋酸根离子个数,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的应用,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系是解题关键,注意甲醛分子结构特点,题目难度不大.

练习册系列答案
相关题目
17.空气污染已成为人类社会面临的重大威胁.下列气体中,不会造成空气污染的是( )
| A. | NO2 | B. | Cl2 | C. | N2 | D. | SO2 |
15.A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍.B在D中充分燃烧能生成其最高价化合物BD2.E+与D2-具有相同的电子数.A在F中燃烧,产物溶于水得到一种强酸.
(1)A在周期表位置第一周期第IA族,写出一种工业制备单质F的离子方程式:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为纯碱(或苏打),其水溶液与F单质反应的化学方程式为Cl2+2Na2CO3+H2O═NaClO+NaCl+2NaHCO3.
(3)由这些元素组成的物质,其组成和结构信息如表:
a的化学式为NaH;b的化学式为Na2O2和Na2C2;c的电子式为 ,d是金属晶体
,d是金属晶体
(4)由A和B元素组成的二元化合物是 沼气的主要成分,其与氧气在酸性电解质溶液中组成燃料电池消耗标况下11.2L氧气时转移电子数为2mol.
(1)A在周期表位置第一周期第IA族,写出一种工业制备单质F的离子方程式:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为纯碱(或苏打),其水溶液与F单质反应的化学方程式为Cl2+2Na2CO3+H2O═NaClO+NaCl+2NaHCO3.
(3)由这些元素组成的物质,其组成和结构信息如表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
 ,d是金属晶体
,d是金属晶体(4)由A和B元素组成的二元化合物是 沼气的主要成分,其与氧气在酸性电解质溶液中组成燃料电池消耗标况下11.2L氧气时转移电子数为2mol.
2.废铅蓄电池的一种回收利用工艺流程如图所示: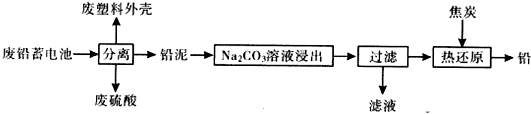
部分难溶电解质的性质如表:
回答下列问题:
(1)废铅蓄电池需回收处理的原因是金属资源的回收(或铅等重金属会引起污染、酸污染等)(回答一点)
(2)将废硫酸和滤液合并后可提取一种钠盐副产品(相对分子质量为322),已知副产品带10个结晶水的结晶水合物,则其化学式Na2SO4•10H2O,由滤液提取该副产品的主要实验步骤依次为蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(3)利用铅泥中的PbSO4溶于CH3COONa溶液生成可溶于水的(CH3COO)2Pb,(CH3COO)2Pb溶液与KClO在强碱性条件下反应制取PbO2,写出后一步生成PbO2的离子方程式CH3COO)2Pb+ClO-+2OH-=Pb02↓+Cl-+2CH3COO-+H2O.
(4)25℃时,Na2CO3溶液浸出时发生反应为:CO32-(aq)+PbSO4(s)?PbCO3(s)+SO42-(aq).测得滤液中c(CO32-)=1×10-5mol/L计算c(SO42-)=1.2mol/L
(5)滤渣PbCO3和焦炭共热可制得金属铅,写出该化学方程式2PbCO3+C$\frac{\underline{\;\;△\;\;}}{\;}$2Pb+3CO2(或PbCO3+2C$\frac{\underline{\;\;△\;\;}}{\;}$Pb+3CO)
(6)已知Pb(OH)2是既能溶于稀硝酸,又能溶于KOH溶液的两性氢氧化物.利用题目所给信息,设计实验区别PbCrO4和BaCrO4:取少量待测物于两支试管中,分别与过量KOH溶液反应,能溶解的是PbCr04,不溶解的是BaCr04.

部分难溶电解质的性质如表:
| 物质 | Ksp(25℃) | 颜色 |
| PbSO4 | 1.8×10-8 | 白色 |
| PbCO3 | 1.5×10-13 | 白色 |
| PbCrO4 | 1.8×10-14 | 黄色 |
| BaCrO4 | 1.2×10-10 | 黄色 |
| Pb(OH)2 | 1.4×10-20 | 白色 |
(1)废铅蓄电池需回收处理的原因是金属资源的回收(或铅等重金属会引起污染、酸污染等)(回答一点)
(2)将废硫酸和滤液合并后可提取一种钠盐副产品(相对分子质量为322),已知副产品带10个结晶水的结晶水合物,则其化学式Na2SO4•10H2O,由滤液提取该副产品的主要实验步骤依次为蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(3)利用铅泥中的PbSO4溶于CH3COONa溶液生成可溶于水的(CH3COO)2Pb,(CH3COO)2Pb溶液与KClO在强碱性条件下反应制取PbO2,写出后一步生成PbO2的离子方程式CH3COO)2Pb+ClO-+2OH-=Pb02↓+Cl-+2CH3COO-+H2O.
(4)25℃时,Na2CO3溶液浸出时发生反应为:CO32-(aq)+PbSO4(s)?PbCO3(s)+SO42-(aq).测得滤液中c(CO32-)=1×10-5mol/L计算c(SO42-)=1.2mol/L
(5)滤渣PbCO3和焦炭共热可制得金属铅,写出该化学方程式2PbCO3+C$\frac{\underline{\;\;△\;\;}}{\;}$2Pb+3CO2(或PbCO3+2C$\frac{\underline{\;\;△\;\;}}{\;}$Pb+3CO)
(6)已知Pb(OH)2是既能溶于稀硝酸,又能溶于KOH溶液的两性氢氧化物.利用题目所给信息,设计实验区别PbCrO4和BaCrO4:取少量待测物于两支试管中,分别与过量KOH溶液反应,能溶解的是PbCr04,不溶解的是BaCr04.
12.钠与水反应的现象与钠的下列性质无关的是( )
| A. | 钠的熔点较低 | B. | 钠的密度小于水 | C. | 钠的硬度较小 | D. | 钠很活泼 |
19.下列物质中能够导电而且是电解质的是( )
| A. | 熔融的氢氧化钠 | B. | 稀盐酸 | C. | 硝酸钾晶体 | D. | 熔化的铁 |
16.从海水提取溴的过程中,吸收塔内溴蒸气和吸收剂SO2发生的化学反应为:Br2+SO2+2H2O=2HBr+H2SO4,下列说法正确的是( )
| A. | SO2在反应中被还原 | B. | Br2在反应中失去电子 | ||
| C. | Br2在反应中表现氧化性 | D. | 1mol氧化剂在反应中得到1mol电子 |
17.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol氮气中所含的氮原子数是0.1NA | |
| B. | 标准状况下,2.24 L乙醇中所含的分子数是0.1NA | |
| C. | 1mol•L-1 氨水溶液中含NH4+的数目是NA | |
| D. | 24g镁和足量的盐酸反应,电子转移的数目是2NA |