题目内容
17.空气污染已成为人类社会面临的重大威胁.下列气体中,不会造成空气污染的是( )| A. | NO2 | B. | Cl2 | C. | N2 | D. | SO2 |
分析 根据物质是否有毒、是否和空气中的物质生成有毒或污染环境的其它物质判断,如高中化学教材中常见有毒气体有:CO、NO、NO2、H2S、SO2、Cl2等,据此进行解答.
解答 解:A.二氧化氮是有刺激性气味的有毒气体,易溶于水生成硝酸,污染大气,故A错误;
B.氯气为黄绿色有毒的气体,会造成环境污染,故B错误;
C.氮气是无色、无味、对环境无污染的气体,故C正确;
D.二氧化硫有刺激性、有毒的气味,能直接危害人体健康,污染大气,故D错误;
故选C.
点评 本题考查了环境污染相关知识,题目难度不大,明确常见污染类型及治理方法为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.起固氮作用的化学反应的是( )
| A. | 工业上用氮气和氢气合成氨气 | B. | 一氧化氮与氧气反应生成二氧化氮 | ||
| C. | 氨气经催化氧化生成一氧化氮 | D. | 由氨气制碳酸氢氨和硫酸氨 |
5.25℃时,在等体积的 ①pH=0的H2SO4溶液、②0.05mol/L的Ba(OH)2溶液、③pH=10的Na2S溶液、④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是( )
| A. | 1:10:1010:109 | B. | 1:5:5×109:5×108 | C. | 5×108:5×109:5:1 | D. | 1010:109:10:1 |
2.下列物质属于油脂的是( )
| A. | 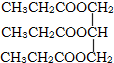 | B. | 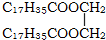 | C. | 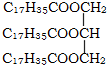 | D. | 润滑油 |
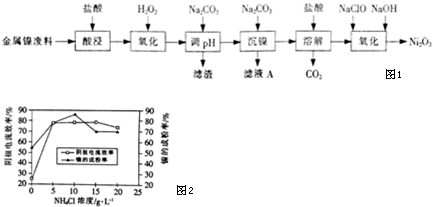
6.NiCl2是化工合成中最重要的镍源,工业上以金属镍废料为原料生产NiCl2,继而生产Ni2O3的工艺流程如图1下:
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
(1)为了提高金属镍废料浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③增大盐酸的浓度(或将镍废料研成粉末等)等.
(2)酸浸后的酸性溶液中含有Ni2+、Cl-,另含有少量Fe2+、Fe3-、Al3+等.沉镍前需加Na2CO3控制溶液pH范围为4.7~7.1.
(3)从滤液A中可回收利用的主要物质是NaCl.
(4)“氧化”生成Ni2O3的离子方程式为2Ni2++ClO-+4OH-=Ni2O3↓+Cl-+2H2O.
(5)工业上用镍为阳极,电解0.05-0.1mol•L-1NiCl2溶液与一定量NH4Cl组成的混合溶液,可得到高纯度、球形的超细镍粉.当其它条件一定时,NH4Cl的浓度对阴极电流效率及镍的成粉率的影响如图2所示.
①NH4Cl的浓度最好控制为10 g•L-1.
②当NH4Cl浓度大于15g•L-1时,阴极有气体生成,导致阴极电流效率降低,写出相应的电极反应式:2H++2e-=H2↑(或2NH4++2H2O+2e-=H2↑+2NH3•H2O).
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Ni(OH)2 |
| 开始沉淀的pH | 1.1 | 6.5 | 3.5 | 7.1 |
| 沉淀完全的pH | 3.2 | 9.7 | 4.7 | 9.2 |
(2)酸浸后的酸性溶液中含有Ni2+、Cl-,另含有少量Fe2+、Fe3-、Al3+等.沉镍前需加Na2CO3控制溶液pH范围为4.7~7.1.
(3)从滤液A中可回收利用的主要物质是NaCl.
(4)“氧化”生成Ni2O3的离子方程式为2Ni2++ClO-+4OH-=Ni2O3↓+Cl-+2H2O.
(5)工业上用镍为阳极,电解0.05-0.1mol•L-1NiCl2溶液与一定量NH4Cl组成的混合溶液,可得到高纯度、球形的超细镍粉.当其它条件一定时,NH4Cl的浓度对阴极电流效率及镍的成粉率的影响如图2所示.
①NH4Cl的浓度最好控制为10 g•L-1.
②当NH4Cl浓度大于15g•L-1时,阴极有气体生成,导致阴极电流效率降低,写出相应的电极反应式:2H++2e-=H2↑(或2NH4++2H2O+2e-=H2↑+2NH3•H2O).

7.设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 1 mol Cl2溶于水的过程中有1NA个电子转移 | |
| B. | 100℃时,1L pH=1的硫酸溶液中,含有0.1NA个H+ | |
| C. | 常温常压下,15g HCHO含有1.5NA对共用电子对 | |
| D. | 0.1mol•L-1的醋酸溶液中CH3COO-少于0.1NA个 |