题目内容
15.A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍.B在D中充分燃烧能生成其最高价化合物BD2.E+与D2-具有相同的电子数.A在F中燃烧,产物溶于水得到一种强酸.(1)A在周期表位置第一周期第IA族,写出一种工业制备单质F的离子方程式:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为纯碱(或苏打),其水溶液与F单质反应的化学方程式为Cl2+2Na2CO3+H2O═NaClO+NaCl+2NaHCO3.
(3)由这些元素组成的物质,其组成和结构信息如表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
 ,d是金属晶体
,d是金属晶体(4)由A和B元素组成的二元化合物是 沼气的主要成分,其与氧气在酸性电解质溶液中组成燃料电池消耗标况下11.2L氧气时转移电子数为2mol.
分析 A,B,D,E,F为短周期元素,非金属元素A最外层电子数与其周期数相同,则A为H;B的最外层电子数是其所在周期数的2倍,则B为C或S,B在D中充分燃烧能生成其最高价化合物BD2,则D为O,B的最高正价为+4价,则B为C;E+与D2-具有相同的电子数,则E为Na;A在F中燃烧,产物溶于水得到种强酸,则F为Cl;
(1)根据H在周期表中的位置分析;工业上常用电解饱和食盐水的方法来制备氯气;
(2)C、O、Na组成的化合物为碳酸钠;碳酸钠与氯气反应生成氯化钠、次氯酸钠、碳酸氢钠;次氯酸钠能与KI反应生成碘单质;
(3)这几种元素只有Na能与H形成离子化合物;根据常见的氧的化合物和碳的化合物分析;根据COCl2结构式分析;只存在一种类型作用力且可导电的单质晶体为Na;
(4)由A和B元素组成的二元化合物是 沼气的主要成分,为CH4,该燃料电池中,通入甲烷的电极是负极、通入氧气的电极是正极,根据氧气和转移电子之间的关系式计算.
解答 解:A,B,D,E,F为短周期元素,非金属元素A最外层电子数与其周期数相同,则A为H;B的最外层电子数是其所在周期数的2倍,则B为C或S,B在D中充分燃烧能生成其最高价化合物BD2,则D为O,B的最高正价为+4价,则B为C;E+与D2-具有相同的电子数,则E为Na;A在F中燃烧,产物溶于水得到种强酸,则F为Cl;
(1)已知A为H在周期表中位于第一周期ⅠA族;工业上常用电解饱和食盐水的方法来制备氯气,其电解离子方程式为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑;
故答案为:第一周期ⅠA族;2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑;
(2)C、O、Na组成的一种盐中,Na的质量分数为43%,则为碳酸钠,其俗名为纯碱(或苏打);碳酸钠与氯气反应生成氯化钠、次氯酸钠、碳酸氢钠,反应的化学方程式为:2Na2CO3+Cl2+H2O═NaCl+NaClO+2NaHCO3,
故答案为:纯碱(或苏打);2Na2CO3+Cl2+H2O═NaCl+NaClO+2NaHCO3;
(3)这几种元素只有Na能与H形成离子化合物,则a的化学式为NaH;含有非极性共价键的二元离子化合物,且原子数之比为1:1,则为Na2O2和Na2C2;已知COCl2结构式为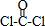 ,则其电子式为
,则其电子式为 ;只存在一种类型作用力且可导电的单质晶体为Na,Na属于金属晶体;
;只存在一种类型作用力且可导电的单质晶体为Na,Na属于金属晶体;
故答案为:NaH;Na2O2和Na2C2; ;金属;
;金属;
(4)由A和B元素组成的二元化合物是 沼气的主要成分,为CH4,该燃料电池中,通入甲烷的电极是负极、通入氧气的电极是正极,根据氧气和转移电子之间的关系式得转移电子物质的量=$\frac{11.2L}{22.4L/mol}×4$=2mol,
故答案为:2.
点评 本题考查位置结构性质的相互关系及运用,为高频考点,综合性较强,涉及元素推断、物质推断、原电池原理、化学用语等知识点,正确推断元素及物质、明确物质结构特点及基本原理是解本题关键,题目难度不大.

| A. | 1:10:1010:109 | B. | 1:5:5×109:5×108 | C. | 5×108:5×109:5:1 | D. | 1010:109:10:1 |
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Ni(OH)2 |
| 开始沉淀的pH | 1.1 | 6.5 | 3.5 | 7.1 |
| 沉淀完全的pH | 3.2 | 9.7 | 4.7 | 9.2 |
(2)酸浸后的酸性溶液中含有Ni2+、Cl-,另含有少量Fe2+、Fe3-、Al3+等.沉镍前需加Na2CO3控制溶液pH范围为4.7~7.1.
(3)从滤液A中可回收利用的主要物质是NaCl.
(4)“氧化”生成Ni2O3的离子方程式为2Ni2++ClO-+4OH-=Ni2O3↓+Cl-+2H2O.
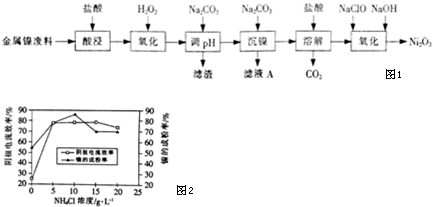
(5)工业上用镍为阳极,电解0.05-0.1mol•L-1NiCl2溶液与一定量NH4Cl组成的混合溶液,可得到高纯度、球形的超细镍粉.当其它条件一定时,NH4Cl的浓度对阴极电流效率及镍的成粉率的影响如图2所示.
①NH4Cl的浓度最好控制为10 g•L-1.
②当NH4Cl浓度大于15g•L-1时,阴极有气体生成,导致阴极电流效率降低,写出相应的电极反应式:2H++2e-=H2↑(或2NH4++2H2O+2e-=H2↑+2NH3•H2O).
| A. | Al是该电池的正极 | B. | H2O2在石墨电极上发生氧化反应 | ||
| C. | 石墨电极附近溶液的pH增大 | D. | 海水中的Cl-向正极移动 |
| A. | 1 mol Cl2溶于水的过程中有1NA个电子转移 | |
| B. | 100℃时,1L pH=1的硫酸溶液中,含有0.1NA个H+ | |
| C. | 常温常压下,15g HCHO含有1.5NA对共用电子对 | |
| D. | 0.1mol•L-1的醋酸溶液中CH3COO-少于0.1NA个 |
 某溶液中可能存在Mg2+、Fe2+、Fe3+,加入NaOH溶液,开始时有白色絮状沉淀生成,白色沉淀迅速变成灰绿色,最后变成红褐色,下列结论正确的是( )
某溶液中可能存在Mg2+、Fe2+、Fe3+,加入NaOH溶液,开始时有白色絮状沉淀生成,白色沉淀迅速变成灰绿色,最后变成红褐色,下列结论正确的是( )| A. | 一定有Fe2+,一定没有Fe3+、Mg2+ | |
| B. | 一定有Fe3+,一定没有Fe2+、Mg2+ | |
| C. | 一定有Fe3+,可能有Fe2+,一定没有Mg2+ | |
| D. | 一定有Fe2+,可能有Mg2+,一定没有Fe3+ |
| A. | 1.5g甲基(-CH3)所含电子数目为NA | |
| B. | 标准状况下,11.2L苯中含有1.5NA 个碳碳双键 | |
| C. | 常温常压下,14 g乙烯和丙烯(C3H6)的混合气体中所含原子总数为3NA | |
| D. | 4.6 g Na与100 mL1.0 mol/L醋酸溶液反应,转移电子数目为0.1NA |
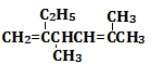 3,5-二甲基-2-乙基-1,4-己二烯.
3,5-二甲基-2-乙基-1,4-己二烯.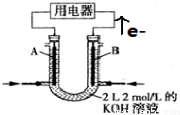 将CH4设计成燃料电池,装置如图所示(A、B为多孔碳棒)
将CH4设计成燃料电池,装置如图所示(A、B为多孔碳棒)