题目内容
11.下列各组离子在强碱性溶液中,可以大量共存的是( )| A. | Na+、Ba2+、AlO2-、NO3- | B. | K+、Na+、HSO3-、Cl- | ||
| C. | NH4+、K+、Cl-、NO3- | D. | Fe3+、Na+、ClO-、S2- |
分析 A.四种离子之间不反应,都不与强碱性溶液中的氢氧根离子反应;
B.亚硫酸氢根离子与强碱性溶液中的氢氧根离子反应;
C.铵根离子与强碱性溶液反应;
D.铁离子、次氯酸根离子与与硫离子反应,铁离子还与强碱性溶液反应.
解答 解:A.Na+、Ba2+、AlO2-、NO3-之间不反应,都不与碱性溶液中的氢氧根离子反应,在溶液中能够大量共存,故A正确;
B.HSO3-与强碱性溶液反应,在溶液中不能大量共存,故B错误;
C.NH4+与强碱性溶液反应,在溶液中不能大量共存,故C错误;
D.Fe3+、ClO-与S2-之间发生反应,Fe3+与强碱性溶液中的氢氧根离子反应,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的正误判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
1.下列反应的离子方程式正确的是( )
| A. | 氯化铝溶液加入过量氨水:Al3++3OH-═Al(OH)3↓ | |
| B. | 稀盐酸滴在石灰石上:CO32-+2H+═CO2↑+H2O | |
| C. | 碳酸氢钠和稀硫酸反应:HCO3-+H+═CO2↑+H2O | |
| D. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- |
2.下列溶液与20mL1 mol•L-1NaNO3溶液中NO3-物质的量浓度相等的是( )
| A. | 10 mL 1mol•L-1Mg(NO3)2 溶液 | B. | 5 mL 0.8mol•L-1 Al(NO3)3溶液 | ||
| C. | 10 mL 2mol•L-1AgNO3溶液 | D. | 10 mL 0.5mol•L-1 Cu(NO3)2溶液 |
19.在xR++yH++O2═mR2++nH2O离子反应方程式中,m 的值是多少( )
| A. | 2x | B. | 4 | C. | 2y | D. | 2 |
16.合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.现将1molN2(g)、3molH2(g)充入一容积为2L的密闭容器中,在500℃下进行反应,10min时达到平衡,NH3的体积分数为φ,下列说法中正确的是( )
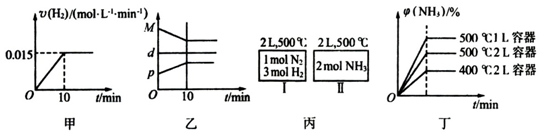

| A. | 若达到平衡时,测得体系放出9.24kJ热量,则H2反应速率变化曲线如图甲所示 | |
| B. | 反应过程中,混合气体平均相对分子质量为M,混合气体密度为d,混合气体压强为p,三者关系如图乙 | |
| C. | 如图丙所示,容器I和II达到平衡时,NH3的体积分数为φ,则容器I放出热量与容器II吸收热量之和为92.4kJ | |
| D. | 若起始加入物料为1 mol N2,3 mol H2,在不同条件下达到平衡时,NH3的体积分数变化如图丁所示 |
3.在不同条件下分别测得反应2SO2+O2?2SO3的化学反应速率,其中表示该反应进行得最快的是( )
| A. | V(SO2)=4mol•L-1•min-1 | B. | V(O2)=3mol•L-1•min-1 | ||
| C. | V(SO3)=0.1mol•L-1•S-1 | D. | V(O2)=0.1mol•L-1•S-1 |