题目内容
19.在xR++yH++O2═mR2++nH2O离子反应方程式中,m 的值是多少( )| A. | 2x | B. | 4 | C. | 2y | D. | 2 |
分析 反应xR++yH++O2=mR2++nH2O中,R的化合价升高,被氧化,O的化合价降低,被还原,根据氧化还原反应得失电子数目相等配平化学方程式,可求m值.
解答 解:反应xR++yH++O2=mR2++nH2O中,R的化合价有+1价升高为+2价,被氧化,O的化合价由0价降低降低到-2价,被还原,根据氧化还原反应中氧化剂和还原剂之间得失电子数目相等,可配平反应的方程式为4R++4H++O2=4R2++2H2O,
则m=4,
故选B.
点评 本题考查氧化还原反应,题目难度不大,注意从质量守恒和得失电子的角度解答,或直接配平方程式,也可得出m.

练习册系列答案
相关题目
9.关于“用CCl4萃取碘的饱和水溶液中的碘”的实验,下列说法正确的是( )
| A. | 使用的实验仪器是容量瓶和烧杯 | |
| B. | 静置后所得液体上层呈紫红色 | |
| C. | 碘在CCl4中的溶解度比在水中的溶解度小 | |
| D. | 如果把CCl4加入碘的不饱和水溶液中,萃取碘的实验也可以成功 |
10.茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是( )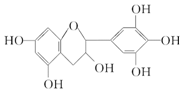

| A. | 分子式为C15H16O7 | |
| B. | 1 mol儿茶素A在一定条件下最多能与6 mol H2加成 | |
| C. | 等质量的儿茶素A分别与足量的金属钠和氢氧化钠反应消耗金属钠和氢氧化钠的物质的量之比为1:1 | |
| D. | 1 mol儿茶素A与足量的浓溴水反应,最多消耗Br2 4 mol |
7.下列变化中必须加入氧化剂才能发生的是( )
| A. | Na2O→NaOH | B. | Fe→FeCl2 | C. | CuO→Cu | D. | H2O2→H2O |
14.设NA为阿伏加德罗常数的值,则下列说法正确的是( )
| A. | 1mol苯酚中“C═C”的个数为3 NA | |
| B. | 常温常压下,22.4L丙烷所含有的共价键数目为10NA | |
| C. | 标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为$\frac{5}{22.4}$ NA | |
| D. | 2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
4.某结晶水合物的化学式为R.xH2O其相对分子质量为M,在25℃时ag晶体溶于bg水中,即达饱和,形成VmL溶液,则下列表达式中不正确的是( )
| A. | 饱和溶液的密度$\frac{(a+b)}{V}$ | |
| B. | 饱和溶液的物质的量浓度$\frac{100a(M-18x)}{MV}$ | |
| C. | 25℃,R的溶解度$\frac{100a(M-18x)}{(bM+18ax)}$ | |
| D. | 饱和溶液的质量分数$\frac{a(M-18x)}{(a+b)M}$ |
11.下列各组离子在强碱性溶液中,可以大量共存的是( )
| A. | Na+、Ba2+、AlO2-、NO3- | B. | K+、Na+、HSO3-、Cl- | ||
| C. | NH4+、K+、Cl-、NO3- | D. | Fe3+、Na+、ClO-、S2- |
8.不能用磨口玻璃塞的试剂瓶盛装的溶液是( )
| A. | CuSO4 | B. | NaOH | C. | AgNO3 | D. | NaCl |