题目内容
单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点越高.下列溶液中沸点最高的是( )
| A、0.01 mol/L的蔗糖溶液 |
| B、0.01 mol/L的K2SO4溶液 |
| C、0.02 mol/L的NaCl溶液 |
| D、0.02 mol/L的CH3COOH溶液 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:根据溶液中非挥发性溶质的分子或离子数越多,该溶液的沸点就越高,则假设溶液为1L时计算选项中溶质的物质的量来比较即可解答.
解答:
解:A、因1L蔗糖溶液中蔗糖的物质的量为1L×0.01mol/L=0.01mol;
B、因1LK2SO4溶液溶质的离子的总物质的量为1L×0.01mol/L×3=0.03mol;
C、因1LNaCl溶液中溶质的离子的总物质的量为1L×0.02mol/L×2=0.04mol;
D、因CH3COOH是挥发性溶质,且1L溶液中分子的物质的量为1L×0.02mol/L=0.02mol,则D不符合题意;
显然C中含0.04 mol离子,离子数最多,
故选:C.
B、因1LK2SO4溶液溶质的离子的总物质的量为1L×0.01mol/L×3=0.03mol;
C、因1LNaCl溶液中溶质的离子的总物质的量为1L×0.02mol/L×2=0.04mol;
D、因CH3COOH是挥发性溶质,且1L溶液中分子的物质的量为1L×0.02mol/L=0.02mol,则D不符合题意;
显然C中含0.04 mol离子,离子数最多,
故选:C.
点评:本题考察角度新颖,利用非挥发性溶质的分子或离子数来判断溶液的沸点高低,学生熟悉物质的量浓度的有关计算是解答的关键,并会判断挥发性物质来解答即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列做法存在安全隐患的是( )
①将水沿着烧杯内壁缓缓加入浓硫酸中,并用玻璃棒不断搅拌;
②取用金属Na或K时,用剩的药品要放回原瓶;
③夜间厨房发生煤气泄漏时,应立即开灯检查煤气泄漏原因,并打开所有门窗通风;
④汞挥发的蒸气有毒性,当汞洒落在地面时,可以在其洒落的地面上洒上硫粉已便除去汞;
⑤废旧电池应回收处理.
①将水沿着烧杯内壁缓缓加入浓硫酸中,并用玻璃棒不断搅拌;
②取用金属Na或K时,用剩的药品要放回原瓶;
③夜间厨房发生煤气泄漏时,应立即开灯检查煤气泄漏原因,并打开所有门窗通风;
④汞挥发的蒸气有毒性,当汞洒落在地面时,可以在其洒落的地面上洒上硫粉已便除去汞;
⑤废旧电池应回收处理.
| A、全部 | B、①④ | C、①③ | D、①②④ |
下列叙述正确的是( )
| A、Na在足量O2中燃烧,消耗l mol O2时转移的电子数是4×6.02×1023 |
| B、盐酸和醋酸的混合溶液pH=1,该溶液中c(H+)=0.1 mol/L |
| C、1 L 0.1 mol/L NH4Cl溶液中的NH4+数是0.1×6.02×1023 |
| D、标准状况下2.24 L Cl2中含有0.2 mol 共价键 |
NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA |
| B、0.1 mol/L NH4Cl溶液中Cl-离子数目为0.1 NA |
| C、反应3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol放出热量9.2 kJ时,转移电子0.6 NA |
| D、0.1 mol H2O2分子中含极性共价键数目为0.3 NA |
将SO2气体通入BaCl2 溶液中,没有看到明显现象,再通入一种气体(或加入一种物质),产生一种白色沉淀,该气体(或物质)不可能是( )
| A、Cl2 |
| B、CO2 |
| C、NH3 |
| D、SO3 |
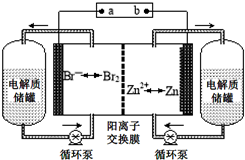 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质储罐和电池间不断循环.下列说法不正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质储罐和电池间不断循环.下列说法不正确的是( )| A、阳离子交换膜可阻止Br2与Zn直接发生反应 |
| B、放电时负极的电极反应式为Zn-2e-=Zn2+ |
| C、充电时电极a连接电源的负极 |
| D、放电时左侧电解质储罐中的离子总浓度增大 |