题目内容
20.下列判断正确的是( )| A. | 取样品进行焰色反应,火焰显黄色,说明有Na元素存在,无K元素 | |
| B. | 向某溶液中滴入稀盐酸立即产生使澄清石灰水变浑浊的气体,说明有CO32-存在 | |
| C. | 向某溶液中滴入KSCN溶液不变色,再滴入几滴氯水变红,说明存在Fe2+,无Fe3+ | |
| D. | 向某溶液中滴加过量Ba(0H)2溶液,最终有白色沉淀,说明无Al3+ |
分析 A.观察K的焰色应透过蓝色的钴玻璃;
B.也可能为HCO3-;
C.KSCN溶液不变色,说明一定不含铁离子,再滴入几滴氯水变红,说明生成铁离子;
D.只能说明含有硫酸根离子.
解答 解:A.观察K的焰色应透过蓝色的钴玻璃,则用洁净的铂丝蘸取溶液进行焰色反应,火焰呈黄色,不能确定是否存在K+,故A错误;
B.某溶液中加入稀盐酸产生无色无味、能使澄清石灰水变浑浊的气体,应为二氧化碳,该溶液中可能为HCO3-或CO32-,故B错误;
C.KSCN溶液不变色,说明一定不含铁离子,再滴入几滴氯水变红,说明生成铁离子,则说明存在Fe2+,无Fe3+,故C正确;
D.向某溶液中滴加过量Ba(0H)2溶液,最终有白色沉淀,只能说明含有硫酸根离子,不能确定是否含有Al3+,故D错误.
故选C.
点评 本题考查较为综合,涉及物质的性质的判断,比较等化学实验方案的设计,侧重于化学实验原理和方案的考查,题目难度不大.

练习册系列答案
相关题目
10.下列过程中所发生的化学变化属于加成反应的是( )
| A. | 乙烯通入酸性高锰酸钾溶液中 | |
| B. | 光照射甲烷与氯气的混合气体 | |
| C. | 在镍作催化剂的条件下,苯与氢气反应 | |
| D. | 苯与液溴混合后撒入铁粉 |
11.下列关于浓硝酸和浓硫酸的叙述,正确的是( )
| A. | 常温下都能用铝制容器贮存 | |
| B. | 露置在空气中,容器内酸液的质量都减轻 | |
| C. | 常温下都能与铜较快地反应 | |
| D. | 露置在空气中,容器内溶质的浓度都升高 |
15.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | $\frac{{K}_{W}}{c{(H}^{+})}$=10-13 mol•L-1的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| B. | 含有0.1 mol•L-1 Fe3+的溶液:Na+、K+、SCN-、NO3- | |
| C. | 能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32- | |
| D. | 水电离的c(H+)=1×10-13mol•L-1的溶液中:K+、Na+、AlO2-、CO32- |
5.化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂:
HIn (溶液)?H+(溶液)+In-(溶液)
红色 黄色
浓度为0.02mol/L的下列溶液 (1)盐酸 (2)NaOH溶液 (3)NaHSO4溶液 (4)NaHCO3溶液(5)氨水,其中能使指示剂显红色的是( )
HIn (溶液)?H+(溶液)+In-(溶液)
红色 黄色
浓度为0.02mol/L的下列溶液 (1)盐酸 (2)NaOH溶液 (3)NaHSO4溶液 (4)NaHCO3溶液(5)氨水,其中能使指示剂显红色的是( )
| A. | (1)(4)(5) | B. | (2)(5) | C. | (1)(3) | D. | (2)(3)(5) |
12.下列微粒对一水合氨的电离平衡几乎不产生影响的是( )
| A. | 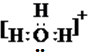 | B. |  | C. |  | D. |  |
13.按图进行实验,试管内充满NO,然后间歇而缓慢地通入一定体积O2,下面有关实验最终状态的描述不正确的是( )

| A. | 若最终有气体剩余,气体呈红棕色 | B. | 若最终有气体剩余,气体是NO | ||
| C. | 试管内溶液为稀的硝酸溶液 | D. | 试管内的液面高度肯定会上升 |