题目内容
5.化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂:HIn (溶液)?H+(溶液)+In-(溶液)
红色 黄色
浓度为0.02mol/L的下列溶液 (1)盐酸 (2)NaOH溶液 (3)NaHSO4溶液 (4)NaHCO3溶液(5)氨水,其中能使指示剂显红色的是( )
| A. | (1)(4)(5) | B. | (2)(5) | C. | (1)(3) | D. | (2)(3)(5) |
分析 能使指示剂显红色,应使溶液中满足:c(HIn)>c(In-),所加入物质应使平衡向逆反应方向移动,所加入溶液应呈酸性,以此解答该题.
解答 解:能使指示剂显红色,应使c(HIn)>c(In-),所加入物质应使平衡向逆反应方向移动,所加入溶液应呈酸性,(1)、(3)为酸性溶液,可使平衡向逆反应方向移动,而(2)、(4)、(5)溶液呈碱性,可使平衡向正反应方向移动,
所以能够使指示剂显红色的是(1)(3),
故选C.
点评 本题考查弱电解质的电离平衡及其影响,题目难度不大,注意根据颜色的变化判断平衡移动的移动方向,结合外界条件对平衡移动的影响分析,试题培养了学生的灵活应用能力.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
20.下列判断正确的是( )
| A. | 取样品进行焰色反应,火焰显黄色,说明有Na元素存在,无K元素 | |
| B. | 向某溶液中滴入稀盐酸立即产生使澄清石灰水变浑浊的气体,说明有CO32-存在 | |
| C. | 向某溶液中滴入KSCN溶液不变色,再滴入几滴氯水变红,说明存在Fe2+,无Fe3+ | |
| D. | 向某溶液中滴加过量Ba(0H)2溶液,最终有白色沉淀,说明无Al3+ |
17.设NA为阿伏加德罗的值,则下列说法正确的是( )
| A. | 标准状况下,22.4L H2S和SO2的混合气体中含有的分子总数为NA | |
| B. | 1 L pH=1的醋酸溶液中,CH3COO-和OH-数目之和为0.1NA | |
| C. | 78g苯中含有碳碳双键的数目为3NA | |
| D. | 6.72L NO2与水充分反应转移的电子数目为0.2NA |
18.类比是研究物质性质的常用方法之一,可预测许多物质的性质.但类比是相对的,不能违背客观实际.下列各说法中正确的是( )
| A. | O2与Cu反应生成CuO,S与Cu反应生成CuS | |
| B. | CaC2能水解:CaC2+2H2O=Ca(OH)2+C2H2↑,则Al4C3也能水解:Al4C3+12H2O═4Al(OH)3+3CH4↑ | |
| C. | 根据化合价Fe3O4可表示为FeO•Fe2O3,则Pb3O4也表示为PbO•Pb2O3 | |
| D. | SO2通入BaCl2溶液不产生沉淀,则SO2通入Ba(NO3)2溶液不产生沉淀 |
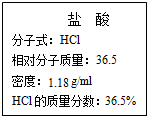 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: