题目内容
根据表中提供的部分短周期元素原子半径及主要化合价的信息,判断以下叙述中正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A、氢化物的沸点为H2T<H2R |
| B、单质与稀盐酸反应的速率为L>Q |
| C、M与T形成的化合物具有两性 |
| D、L2+与R2-的核外电子数相等 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:短周期元素,T、R都有-2价,处于ⅥA族,T只有-2价,则T为O元素、R为S元素,L、Q都有+2价,处于ⅡA族,原子半径L>Q,则L为Mg元素\Q为Be元素,M有+3价,处于ⅢA族,原子半径M的介于L、R之间,则M为Al元素.
解答:
解:短周期元素,T、R都有-2价,处于ⅥA族,T只有-2价,则T为O元素、R为S元素,L、Q都有+2价,处于ⅡA族,原子半径L>Q,则L为Mg元素\Q为Be元素,M有+3价,处于ⅢA族,原子半径M的介于L、R之间,则M为Al元素,
A.非金属性O>S,元素的非金属性越强,对应的氢化物越稳定,故A错误;
B.金属性Mg>Be,则Mg与酸反应越剧烈,故B正确;
C.M与T形成的化合物是氧化铝,属于两性氧化物,故C正确;
D.L2+的核外电子数为12-2=10,R2-的核外电子数为16-(-2)=18,不相等,故D错误,
故选BC.
A.非金属性O>S,元素的非金属性越强,对应的氢化物越稳定,故A错误;
B.金属性Mg>Be,则Mg与酸反应越剧烈,故B正确;
C.M与T形成的化合物是氧化铝,属于两性氧化物,故C正确;
D.L2+的核外电子数为12-2=10,R2-的核外电子数为16-(-2)=18,不相等,故D错误,
故选BC.
点评:本题考查元素的性质,学生能利用原子半径及化合价来推断出元素是解答本题的关键,并熟悉元素及其单质、化合物的性质来解答即可,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
将足量NO2通入下列各溶液中,所含离子还能大量共存的是( )
| A、Fe2+、Cl-、SO42-、Na+ |
| B、NH4+、Al3+、NO3-、Cl- |
| C、Ca2+、K+、Cl-、HCO3- |
| D、K+、Na+、SO32-、SO42- |
在2L密闭容器中,保持恒温,加热KClO3和MnO2固体混合物制取O2,5min后,生成O2 32克,则此反应的平均速率可表示为( )
| A、v(O2)=3.2g?L-1?min-1 |
| B、v(O2)=0.1 mol?L-1?min-1 |
| C、v(KCl)=0.1 mol?L-1?min-1 |
| D、v(KClO3)=0.0667 mol?L-1?min-1 |
关于CH4和 的叙述正确的是( )
的叙述正确的是( )
 的叙述正确的是( )
的叙述正确的是( )| A、通常情况下它们都是气态烷烃 |
| B、与所有烷烃互为同系物 |
| C、因为它们结构相似,所以它们的化学性质相似,物理性质相同 |
| D、均能用CnH2n+2组成通式来表示 |
 镁燃料电池具有比能量高、安全方便、成本低等特点,常用的有镁-次氯酸盐燃料电池,镁-过氧化氢燃料电池等,图为镁-次氯酸盐燃料电池的工作原理图,下列说法不正确的是( )
镁燃料电池具有比能量高、安全方便、成本低等特点,常用的有镁-次氯酸盐燃料电池,镁-过氧化氢燃料电池等,图为镁-次氯酸盐燃料电池的工作原理图,下列说法不正确的是( )| A、电池的总反应式为Mg+ClO-+H2O═Mg(OH)2+Cl- |
| B、放电过程中OH-移向正极 |
| C、镁电池中镁均为负极,发生氧化反应 |
| D、镁-过氧化氢燃料电池,酸性电解质中正极反应式为H2O2+2H++2e-═2H2O |

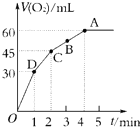 加入0.1mol MnO2粉末于50mL过氧化氢溶液(H2O2,ρ=1.1g?mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.
加入0.1mol MnO2粉末于50mL过氧化氢溶液(H2O2,ρ=1.1g?mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.