题目内容
3.设NA为阿伏加德罗常数的值,下列关于0.2mol/L Ba(NO3)2溶液不正确的说法是( )| A. | 500 mL溶液中的阴、阳离子总数为0.3NA | |
| B. | 500 mL溶液中NO3-离子浓度为0.2mol/L | |
| C. | 500 mL溶液中Ba2+离子浓度为0.2mol/L | |
| D. | 500 mL溶液中NO3-离子总数为0.2NA |
分析 A、求出500mL溶液中Ba(NO3)2的物质的量,然后根据1molBa(NO3)2含3mol离子来分析;
B、NO3-离子浓度与所取溶液的体积无关;
C、Ba2+离子浓度与所取溶液体积无关;
D、求出500mL溶液中Ba(NO3)2的物质的量,然后根据1molBa(NO3)2含2molNO3-离子来分析.
解答 解:A、500mL溶液中Ba(NO3)2的物质的量n=CV=0.2mol/L×0.5L=0.1mol,而1molBa(NO3)2含3mol离子,故0.1mol硝酸钡中含0.3mol离子即0.3NA个,故A正确;
B、NO3-离子浓度与所取溶液的体积无关,即0.2mol/L Ba(NO3)2溶液中硝酸根的浓度为0.4mol/L,故B错误;
C、Ba2+离子浓度与所取溶液体积无关,即0.2mol/L Ba(NO3)2溶液中钡离子的浓度为0.2mol/L,故C正确;
D、500mL溶液中Ba(NO3)2的物质的量n=CV=0.2mol/L×0.5L=0.1mol,而1molBa(NO3)2含2molNO3-离子,故0.1mol硝酸钡中含0.2NA个硝酸根,故D正确.
故选B.
点评 本题考查了溶液中离子浓度和个数的计算,应注意的是当溶液浓度一定时,离子浓度和所取溶液的体积无关.

练习册系列答案
 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
13.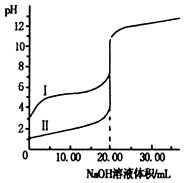 室温下,用0.1mol•L-1 NaOH溶液分别滴定20.00ml0.1mol•L-1的盐酸和醋酸溶液,滴定曲线如图.下列说法正确的是( )
室温下,用0.1mol•L-1 NaOH溶液分别滴定20.00ml0.1mol•L-1的盐酸和醋酸溶液,滴定曲线如图.下列说法正确的是( )
 室温下,用0.1mol•L-1 NaOH溶液分别滴定20.00ml0.1mol•L-1的盐酸和醋酸溶液,滴定曲线如图.下列说法正确的是( )
室温下,用0.1mol•L-1 NaOH溶液分别滴定20.00ml0.1mol•L-1的盐酸和醋酸溶液,滴定曲线如图.下列说法正确的是( )| A. | I、Ⅱ分别表示盐酸和醋酸的滴定曲线 | |
| B. | V(NaOH)=10.00mL时,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$>1 | |
| C. | pH=7时,两种酸所消耗NaOH溶液的体积相等 | |
| D. | V(NaOH)=20.00mL时,c(Cl一)<c(CH3COO一) |
18.硅芯片是各种计算机、微电子产品的核心.工业上通过以下反应将自然界的二氧化硅转化为硅:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,下列针对该反应的分析不正确的是( )
| A. | 属于置换反应 | B. | 碳发生了还原反应 | ||
| C. | 二氧化硅是氧化剂 | D. | 24g碳充分反应生成28g硅 |
8. 已知:乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
已知:乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
【观察与思考】
(1)乙醇分子的核磁共振氢谱有3个吸收峰.
【活动与探究】
(2)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现象.
请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不规定填满).
(3)乙同学向试管中加入3~4mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,反复多次,写出发生反应的化学方程式:2CH3CH2OH+O22$→_{△}^{Cu}$CH3CHO+2H2O;欲验证此实验的有机产物,可以将产物加入盛有新制的氢氧化铜悬浊液的试管中并在酒精灯火焰上直接加热煮沸,可观察到有砖红色沉淀产生.
【交流与讨论】
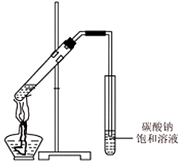
(4)丙同学向一支试管中加入3mL 乙醇,然后边摇动试管边慢慢加入2mL浓硫酸和2mL冰醋酸,按如图所示连接好装置,
请指出该装置的主要错误是导管插入到饱和碳酸钠溶液中,写出该反应的化学方程式CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;饱和碳酸钠溶液在本实验的作用是除去乙酸乙酯中的乙酸和乙醇.
 已知:乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
已知:乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.【观察与思考】
(1)乙醇分子的核磁共振氢谱有3个吸收峰.
【活动与探究】
(2)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现象.
请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不规定填满).
| 实验现象 | 结 论 | |
| ① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
【交流与讨论】
(4)丙同学向一支试管中加入3mL 乙醇,然后边摇动试管边慢慢加入2mL浓硫酸和2mL冰醋酸,按如图所示连接好装置,
请指出该装置的主要错误是导管插入到饱和碳酸钠溶液中,写出该反应的化学方程式CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;饱和碳酸钠溶液在本实验的作用是除去乙酸乙酯中的乙酸和乙醇.
15. 密闭容器中自由移动的活塞两边分别充入空气和H2、O2的混合气体,开始体积比为1:3,若将H2、O2的混合气体点燃引爆,恢复到原来温度(水为液态),活塞右滑停留于容器的正中央,则原来H2、O2的体积比可能为( )
密闭容器中自由移动的活塞两边分别充入空气和H2、O2的混合气体,开始体积比为1:3,若将H2、O2的混合气体点燃引爆,恢复到原来温度(水为液态),活塞右滑停留于容器的正中央,则原来H2、O2的体积比可能为( )
 密闭容器中自由移动的活塞两边分别充入空气和H2、O2的混合气体,开始体积比为1:3,若将H2、O2的混合气体点燃引爆,恢复到原来温度(水为液态),活塞右滑停留于容器的正中央,则原来H2、O2的体积比可能为( )
密闭容器中自由移动的活塞两边分别充入空气和H2、O2的混合气体,开始体积比为1:3,若将H2、O2的混合气体点燃引爆,恢复到原来温度(水为液态),活塞右滑停留于容器的正中央,则原来H2、O2的体积比可能为( )| A. | 1:2 | B. | 3:2 | C. | 5:2 | D. | 7:2 |
7.下列各组溶液,只要用试管和胶头滴管,不用任何化学试剂就可以鉴别的是( )
| A. | HCl和Na2CO3 | B. | 稀H2SO4和NaHCO3 | C. | CaCl2和Na2CO3 | D. | Ba(OH)2和NaHSO4 |