题目内容
13.下列叙述正确的是( )| A. | 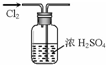 用于干燥氯气 | B. | 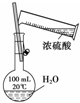 用于配制一定浓度的硫酸溶液 | ||
| C. | 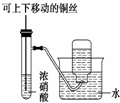 用于制备并收集少量NO2气体 | D. | 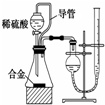 用于测定一定质量镁铝合金的组成 |
分析 A.导管长进短出;
B.浓硫酸不能在容量瓶中稀释;
C.二氧化氮能和水反应;
D.装置可得到生成气体的体积.
解答 解:A.导管长进短出,否则会将液体排除,故A错误;
B.容量瓶是用来配制一定浓度的溶液的专用仪器,瓶颈上有容量刻度,浓硫酸溶于水溶液温度升高,热胀冷缩,影响刻度,影响配制的精确度,所以容量瓶不能用来稀释溶解物质,应在烧杯中溶解浓硫酸,冷却后再转入容量瓶,故B错误;
C.二氧化氮溶于水和水反应生成硝酸和一氧化氮,该实验制备不能收集少量NO2气体,故C错误;
D.装置可得到生成气体的体积,结合合金的质量可计算合金的组成,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及气体干燥收集、溶液的配制以及物质含量的测定等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
3.能正确表示下列反应的离子方程式是( )
| A. | Fe3O4与稀硝酸反应:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| B. | NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| C. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 向FeCl3溶液中加入少量KSCN溶液:Fe3++3SCN-═Fe(SCN)3↓ |
1.下列物质发生反应时,不因为反应的条件、反应物浓度或反应物的用量不同,而产物不同的是( )
| A. | 钠与氧气 | B. | 碳与氧气 | C. | 硅和氯气 | D. | 铁和硫酸 |
18.根据图示转化关系,下列说法不正确是( )
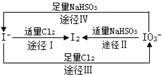

| A. | 由图可知离子还原性的强弱顺序为HSO3->I->Cl- | |
| B. | 足量Cl2能使湿润的淀粉-KI试纸先变蓝后变白 | |
| C. | 途径Ⅱ、Ⅳ反应后溶液的pH均减小 | |
| D. | 途径Ⅲ中若氧化1 mol I-,需消耗67.2L氯气 |
5.某烃的分子式为C4H8,已知它能使酸性KMnO4溶液褪色,完全燃烧时生成等物质的量的CO2与H2O,则它与HBr加成反应时,最多可得到几种不同(不考虑立体异构)的产物( )
| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
1.在一定温度下的定容密闭容器中,当下列物理量不再改变时,不能表明反应A(s)+2B(g)?C(g)+D(g)已达平衡的是( )
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | 混合气体的相对分子质量 | D. | C气体的总物质的量浓度 |
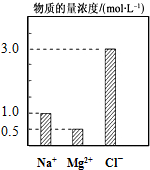 在200mL由NaCl、MgCl2、KCl组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
在200mL由NaCl、MgCl2、KCl组成的混合液中,部分离子浓度大小如图所示,回答下列问题: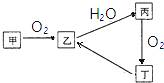 已知甲、乙、丙、丁4种物质均含有常见非金属元素,其中甲为淡黄色粉末.它们之间有如图所示的转化关系(转化过程中部分产物未标出).
已知甲、乙、丙、丁4种物质均含有常见非金属元素,其中甲为淡黄色粉末.它们之间有如图所示的转化关系(转化过程中部分产物未标出).