题目内容
1.下列物质发生反应时,不因为反应的条件、反应物浓度或反应物的用量不同,而产物不同的是( )| A. | 钠与氧气 | B. | 碳与氧气 | C. | 硅和氯气 | D. | 铁和硫酸 |
分析 A.条件不同时,Na和氧气的反应产物不同;
B.碳在氧气中燃烧,氧气不足是生成一氧化碳,氧气足量时生成二氧化碳;
C.硅和氯气反应生成四氯化硅;
D、铁与稀硫酸生成硫酸亚铁和氢气;铁和浓硫酸发生钝化现象.
解答 解;A.条件不同时,Na和氧气的反应产物不同,常温下生成氧化钠,加热时生成过氧化钠,故A不选;
B.碳在氧气中燃烧,氧气不足是生成一氧化碳,氧气足量时生成二氧化碳,与量有关,故B不选;
C.硅和氯气反应生成四氯化硅,不因为反应的条件、反应物浓度或反应物的用量不同,而产物不同,故C选;
D、铁与稀硫酸生成硫酸亚铁和氢气;铁和浓硫酸发生钝化现象,反应的条件、反应物浓度或反应物的用量不同,而产物不同,故D不选;
故选C.
点评 本题考查了反应条件或反应物的用量对反应的影响,多角度考查元素混合物知识,为高频考点,题目难度不大,熟悉物质的性质是解题的关键.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
11.利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间,下列说法不正确的是( )

| A. | a管发生吸氧腐蚀,b管发生析氢腐蚀 | |
| B. | a处溶液的pH增大,b处溶液的pH减小 | |
| C. | 一段时间后,a管液面高于b管液面 | |
| D. | 两侧生铁丝发生相同的电极反应:Fe-2e-═Fe2+ |
12.下列离子方程式书写正确的是( )
| A. | 氧化钠与水反应:O2-+2H2O═2OH- | |
| B. | 氯气通入溴化钠溶液中:Cl2+2Br-═2Cl-+Br2 | |
| C. | 硫酸铜溶液与氢氧化钡溶液混合:SO42-+Ba2+═BaSO4↓ | |
| D. | 氯化亚铁溶液中通入氯气:Fe2++Cl2═Fe3++2Cl- |
9.常温下能与浓硫酸发生剧烈反应的金属单质是( )
| A. | Cu | B. | C | C. | Fe | D. | Mg |
16.在酸性溶液中,下列离子不能大量存在的是( )
| A. | Mg2+ | B. | OHˉ | C. | SO42- | D. | Fe3+ |
6.下列说法正确的是( )
| A. | 镁着火后可用二氧化碳灭火器进行灭火 | |
| B. | 焰色反应时,先用稀硫酸洗涤铂丝并在酒精灯火焰上灼烧,然后再进行实验 | |
| C. | 食盐水中混有Mg2+、Ca2+、SO42-,可依次加入过量Ba(OH)2溶液、Na2CO3溶液和适量盐酸,过滤后即可得到精制的食盐水 | |
| D. | 现代化学分析测试中,常借助一些仪器来分析化学物质的组成.如用原子吸收光谱确定物质中含有哪些金属元素 |
13.下列叙述正确的是( )
| A. | 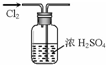 用于干燥氯气 | B. | 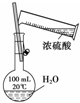 用于配制一定浓度的硫酸溶液 | ||
| C. | 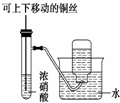 用于制备并收集少量NO2气体 | D. | 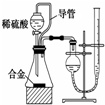 用于测定一定质量镁铝合金的组成 |
10.在3BrF3+5H2O═HBrO3+Br2+9HF+SO2反应中,若有5mol H2O作还原剂,铜被水还原的BrF3的物质的量为( )
| A. | 3mol | B. | 2mol | C. | $\frac{4}{3}$mol | D. | $\frac{10}{3}$mol |