题目内容
8.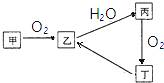 已知甲、乙、丙、丁4种物质均含有常见非金属元素,其中甲为淡黄色粉末.它们之间有如图所示的转化关系(转化过程中部分产物未标出).
已知甲、乙、丙、丁4种物质均含有常见非金属元素,其中甲为淡黄色粉末.它们之间有如图所示的转化关系(转化过程中部分产物未标出).(1)丙的化学式为H2SO3.
(2)写出丁→乙的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
分析 甲、乙、丙、丁4种物质均含有常见非金属元素,其中甲为淡黄色粉末,甲能燃烧,则甲是S,乙为SO2,乙和水反应生成亚硫酸,则丙是H2SO3,丙被氧化生成丁,丁为H2SO4,丁发生氧化还原反应生成乙,据此分析解答.
解答 解:甲、乙、丙、丁4种物质均含有常见非金属元素,其中甲为淡黄色粉末,甲能燃烧,则甲是S,乙为SO2,乙和水反应生成亚硫酸,则丙是H2SO3,丙被氧化生成丁,丁为H2SO4,丁发生氧化还原反应生成乙,
(1)通过以上分析知,丙是亚硫酸,其化学式为H2SO3,故答案为:H2SO3;
(2)在加热条件下,Cu和浓硫酸发生氧化还原反应生成二氧化硫,反应方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
点评 本题以S及其化合物为载体考查无机物推断,为高频考点,明确常见物质特殊性质是解本题关键,知道常见物质之间的转化,知道浓硫酸的强氧化性、吸水性和脱水性等,题目难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
18.在溶液中能大量共存,且加入稀硫酸时,有气体生成的是( )
| A. | Na+、Ag+、CO32-、Cl- | B. | K+、Ba2+、SO42-、Cl- | ||
| C. | Na+、K+、CO32-、Cl- | D. | Na+、K+、Cl-、SO42- |
19.如图是研究二氧化硫性质的微型实验装置(实验时用另一表面皿扣在上面),现用75%硫酸溶液和亚硫酸钠晶体反应制取SO2气体并进行实验,实验现象很明显.下列说法中错误的是( )


| A. | 品红溶液褪色 | B. | 紫色石蕊溶液先变红后褪色 | ||
| C. | 酸性KMnO4溶液紫色褪去 | D. | 含酚酞的NaOH溶液红色变浅 |
16.在酸性溶液中,下列离子不能大量存在的是( )
| A. | Mg2+ | B. | OHˉ | C. | SO42- | D. | Fe3+ |
3.下列离子方程式正确的是( )
| A. | 硫酸铜溶液与氢氧化钡溶液反应:SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓ | |
| B. | 漂白粉溶液在空气中发生的反应:Ca2++2ClO-+CO2+H2O═2HClO+CaCO3↓ | |
| C. | 碳酸钙溶解于盐酸中:CO32-+2H+═CO2↑+H2O | |
| D. | 氯化铁溶液与碘化钾溶液反应:Fe3++2Iˉ═Fe2++I2 |
13.下列叙述正确的是( )
| A. | 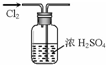 用于干燥氯气 | B. | 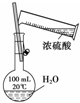 用于配制一定浓度的硫酸溶液 | ||
| C. | 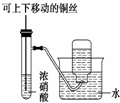 用于制备并收集少量NO2气体 | D. | 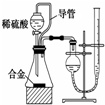 用于测定一定质量镁铝合金的组成 |
20.下列叙述正确的是( )
| A. | 在中和热的测定实验中,应将碱液缓慢倒入酸液中,使反应充分进行 | |
| B. | 除去NaCl中少量的KNO3,可将固体混合物制成热饱和溶液,冷却结晶、过滤 | |
| C. | 将硫代硫酸钠溶液和稀硫酸混合,可通过观察产生气泡的快慢来判断化学反应速率 | |
| D. | 将铁钉放试管中,加入2mL水、3滴稀醋酸和1滴K3[Fe(CN)6]溶液,不久铁钉周围出现蓝色沉淀 |
17.下列离子在溶液中因发生氧化还原反应而不能大量共存的是( )
| A. | H+、NO3-、Fe2+、NH4+ | B. | Ag+、NO3-、Cl-、OH- | ||
| C. | K+、Ba2+、OH-、H+ | D. | NH4+、Br-、OH-、Mg2+ |
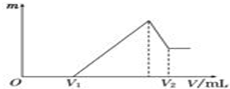 将0.1mol的镁、铝混合物溶于100mL,2mol/L H2SO4溶液中,然后再滴加1mol/L NaOH溶液.请回答:
将0.1mol的镁、铝混合物溶于100mL,2mol/L H2SO4溶液中,然后再滴加1mol/L NaOH溶液.请回答: