题目内容
3.下列化合物中,既含有离子键,又含有非极性共价键的是( )| A. | H2O2 | B. | NaOH | C. | Na2O2 | D. | NH4Cl |
分析 活泼金属元素和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,据此分析解答.
解答 解:A.H2O2是共价化合物,含有极性共价键和非极性共价键,故A错误;
B.NaOH是复杂的离子化合物,含有离子键、极性共价键,故B错误;
C.Na2O2是复杂的离子化合物,含有离子键、非极性共价键,故C正确;
D.NH4Cl是离子化合物,含有离子键、极性共价键,故D错误;
故选C.
点评 本题考查化学键判断,为高频考点,明确离子键和共价键根本区别是解本题关键,注意:配位键属于共价键.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
13.等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则下列说法正确的是( )
| A. | 第一块钠消耗的氧气多 | B. | 两块钠消耗的氧气一样多 | ||
| C. | 第二块钠的反应产物质量大 | D. | 两块钠的反应产物质量一样大 |
11.下列对有机物结构的叙述中不正确的是( )
| A. | 硝基、羟基、氯原子、苯环、甲基都是官能团 | |
| B. | 邻二甲苯不存在同分异构体,说明苯分子中所有的碳碳键都是完全相同的 | |
| C. | 乙烯、苯分子中所有原子共平面 | |
| D. | CH2Cl2有两种同分异构体 |
18.下列过程中,不涉及化学变化的是( )
| A. | 浓硫酸加入蔗糖固体中 | B. | SO2使品红溶液褪色 | ||
| C. | 四氯化碳萃取碘水中的碘 | D. | 氨气溶于水,水溶液呈碱性 |
8.下列有机反应方程式书写正确且属于取代反应的是( )
| A. | CH2=CH2+Br2→CH2BrCH2Br | B. | 2CH3CH3+Cl2$\stackrel{光照}{→}$2CH3CH2Cl+H2 | ||
| C. | CH3CH2OH+Na→CH3CH2ONa+H2↑ | D. | 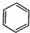 +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$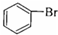 +HBr +HBr |
15.设NA为阿伏加罗常数的数值,下列说法正确的是( )
| A. | 1.6g臭氧中含有的氧原子数为0.1NA | |
| B. | 18gD2O中含有的质子数为10NA | |
| C. | 50mL12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| D. | 标准状况下,11.2L己烷含有的分子数为0.5NA |
12.反应4A (s)+3B (g)?2C (g)+D (g),经2min,B的浓度减少0.6mol/L,对此下列说法不正确的是( )
| A. | 在2 min内的反应速率用B表示为0.3 mol/(L•min) | |
| B. | 在2 min内用A表示反应速率是0.4 mol/(L•min) | |
| C. | 在2 min内用C表示反应速率是0.2 mol/(L•min) | |
| D. | 当V正(B)=3V逆(D)时,反应达到平衡 |
13.设NA表示阿伏加德罗常数的数值,下列说法中,不正确的是( )
| A. | 标准状况下,22.4L氢气和氧气的混合气体,所含分子数为NA | |
| B. | 常温常压下,1mol氦气含有的原子数为2NA | |
| C. | 1molAl3+含有核外电子数为10NA | |
| D. | 17gNH3含有的电子数为10NA |