题目内容
9.1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18克/厘米3,沸点131.4℃,熔点9.79℃,溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验中可以用下图所示装置制备1,2-二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有浓溴(表面覆盖少量水).请填写下列空白: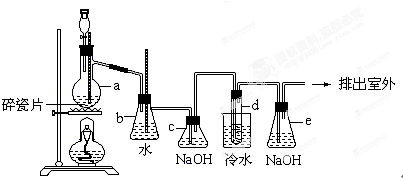
(1)烧瓶a中发生的是乙醇的脱水反应,即消去反应,反应温度是170℃,并且该反应要求温度迅速升高到170℃,否则容易产生副反应.请你写出乙醇的这个消去反应方程式:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.
(2)写出制备1,2-二溴乙烷的化学方程式:CH2=CH2+Br2→CH2BrCH2Br.
(3)安全瓶b可以以上倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象b中水面会下降,玻璃管中的水柱会上升,甚至溢出.
(4)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因.①乙烯流速过快,未完全发生加成反应、②实验过程中,乙烯和浓硫酸的混合液没有迅速达到170℃,发生副反应生成乙醚.
(5)c装置内NaOH溶液的作用是吸收乙烯气体中含有的CO2、SO2等酸性气体;e装置内NaOH溶液的作用是吸收HBr和Br2等气体,防止大气污染.
分析 (1)乙醇在浓硫酸做催化剂、脱水剂条件下发生消去反应生成乙烯,必须注意反应温度;
(2)乙烯与液溴发生加成反应生成1,2-二溴乙烷;
(3)依据当d堵塞时,气体不畅通,则在b中气体产生的压强将水压入直玻璃管中,甚至溢出玻璃管;
(4)根据乙烯与溴反应的利用率减少的可能原因进行解答;
(5)c中的氢氧化钠可以和制取乙烯中产生的杂质气体二氧化碳和二氧化硫发生反应;反应剩余的溴化氢、溴等有毒,能够污染大气,需要进行尾气吸收,用e吸收.
解答 解:(1)乙醇在170℃时发生消去生成乙烯,温度必须是170℃,反应方程式为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;
(2)乙烯与液溴发生加成反应生成1,2-二溴乙烷化学方程式为:CH2=CH2+Br2→CH2BrCH2Br,
故答案为:CH2=CH2+Br2→CH2BrCH2Br;
(3)试管d发生堵塞时,b中压强不断增大,会导致b中水面下降,玻璃管中的水柱上升,甚至溢出,
故答案为:b中水面会下降,玻璃管中的水柱会上升,甚至溢出;
(4)当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多的原因可能是乙烯发生(或通过液溴)速度过快,导致大部分乙烯没有和溴发生反应;此外实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃会导致副反应的发生和副产物的生成,
故答案为:①乙烯流速过快,未完全发生加成反应、②实验过程中,乙烯和浓硫酸的混合液没有迅速达到170℃,发生副反应生成乙醚;
(5)装置c中盛有氢氧化钠可以和制取乙烯中产生的杂质气体二氧化碳和二氧化硫发生反应;
该反应中剩余的溴化氢及反应副产物溴单质等有毒,会污染大气,应该进行尾气吸收,所以装置e中氢氧化钠溶液的作用是吸收HBr和Br2等气体,防止大气污染,
故答案为:吸收乙烯气体中含有的CO2、SO2等酸性气体;吸收HBr和Br2等气体,防止大气污染.
点评 本题考查了制备实验方案的设计、溴乙烷的制取方法,题目难度中等,注意掌握溴乙烷的制取原理、反应装置选择及除杂、提纯方法,培养学生分析问题、理解能力及化学实验能力.

| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||||||||||||
| ⑪ | ⑫ | ||||||||||||||||
(2)画出⑨的简单离子的结构示意图
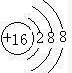 .
.(3)①②⑤⑧的原子半径由大到小的顺序是Na>Si>C>H(用元素符号表示).
(4)②⑧⑨⑩的最高价氧化物的水化物的酸性由强到弱的顺序是HClO4>H2SO4>H2CO3>H2SiO3(用化学式表示).
(5)⑤与⑦的最高价氧化物的水化物间反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(6)⑨⑩的简单离子半径由大到小的顺序是S2->Cl-(用离子符号表示).
(7)⑩的非金属性比⑫强,用一个离子方程式表示为2Br-+Cl2=2Cl-+Br2.
(8)用电子式表示⑨与⑪形成化合物的过程为
 .
.(9)③的气态氢化物与其最高价含氧酸反应的产物中化学键的类型是离子键和共价键.
(10)⑥与⑦的金属性较强的是镁(填元素名称).
(11)②的最高价氧化物的电子式为
 .
. | A. | 1-氯丁烷 | B. | 氯乙烷 | C. | 2-氯丁烷 | D. | 溴丙烷 |
| A. | 1L1mol/L的氯化铁溶液中,若C1-的数目为3 NA,则Fe3+的数目为NA | |
| B. | 1 molN2和3 molH2在一定条件下充分反应,转移电子数目为6NA | |
| C. | 常温下,1L0.1mol/L的Na2S溶液中阴离子数目大于0.1 NA | |
| D. | 0.1 mol Cl2通入水中,转移电子的数目为0.1NA |
| 实验操作 | 现象 | 结论 | |
| A | 在淀粉溶液中加入稀硫酸加热一段时间后冷却至室温,再加入碘水. | 溶液变蓝 | 说明淀粉没有水解 |
| B | 将乙醇与酸性重铬酸钾(K2Cr2O7)溶液混合 | 橙色溶液变为绿色 | 乙醇具有还原性 |
| C | 蔗糖溶液中加入稀硫酸,水解后加入银氨溶液,水浴加热 | 未出现银镜 | 水解的产物中没有葡萄糖 |
| D | 将新制Cu(OH)2与葡萄糖溶液混合加热 | 产生红色沉淀(Cu2O) | 葡萄糖具有氧化性 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 键能越大说明化学键越牢固,所构成的物质越稳定 | |
| B. | 高聚氮晶体属于原子晶体 | |
| C. | 该晶体中氮原子数与氮氮键数比为1:3 | |
| D. | 高聚氮可以用作炸药 |
| A. | 滴入石蕊试液显蓝色的溶液中:K+、Na+、HSO3-、ClO- | |
| B. | 0.1mol/L的Fe(NO3)3溶液中:Na+、H+、Cl-、I- | |
| C. | 0.1mol/L的NaAlO2溶液中:K+、H+、NO3-、SO42- | |
| D. | 无色透明的水溶液中:Mg2+、H+、Cl-、SO42- |
 ,B的结构简式
,B的结构简式 或
或 .
. ,反应类型:取代反应.
,反应类型:取代反应.