题目内容
下列有关物质的性质属于物理性质的是( )
| A、硫酸的酸性 |
| B、盐酸的挥发性 |
| C、碳酸的不稳定性 |
| D、氢气的还原性 |
考点:物理变化与化学变化的区别与联系
专题:物质的性质和变化专题
分析:物理性质是指不发生化学变化就表现出来的性质,化学性质是指经过发生化学变化才表现出来的性质,此题关键看有无发生化学变化.
解答:
解:A.硫酸的酸性:能与铁反应生成硫酸亚铁和氢气,属于化学性质,故A错误;
B.盐酸的挥发性:盐酸沸点低,易挥发,属于物理性质,故B正确;
C.碳酸的不稳定性:碳酸受热易分解生成二氧化碳和水,属于化学性质,故C错误;
D.氢气的还原性:氢气能还原氧化铜生成铜和水,属于化学性质,故D错误,
故选B.
B.盐酸的挥发性:盐酸沸点低,易挥发,属于物理性质,故B正确;
C.碳酸的不稳定性:碳酸受热易分解生成二氧化碳和水,属于化学性质,故C错误;
D.氢气的还原性:氢气能还原氧化铜生成铜和水,属于化学性质,故D错误,
故选B.
点评:本题考查物理性质与化学性质的差别及应用,而性质决定变化,变化反映性质,因此主要看其是发生了何种变化.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
铵盐是一类重要的氮的化合物,设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1 mol NH4+含有的电子数为11N A |
| B、NH4+是正四面体的分子 |
| C、0.1 L 3 mol?L-1的NH4NO3溶液中氮原子数等于0.6N A |
| D、将分子总数为NA的NH3和HCl的混合气体置于标准状况下,其体积约为22.4 L |
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4L H2O含有的分子数为NA |
| B、4g NaOH含有的Na+离子数为0.1 NA |
| C、28g N2含有的原子数为NA |
| D、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、用石墨电极电解氯化铜溶液时,若阴极增重64 g,则阳极能产生NA个氯气分子 |
| B、25℃,pH=1的稀硫酸中含有的H+数为0.1 NA |
| C、用石墨电极电解饱和食盐水,当阴极产生2.24 L H2时,转移的电子数一定为0.2 NA |
| D、100 mL 1 mol?L-1的NH4Cl溶液中,NH4+的数目等于0.1 NA |
下列说法正确的是( )
| A、标准状况下,22.4 L己烯含有的分子数约为6.02×1023 |
| B、7.1 g氯气与足量的氢氧化钠溶液反应转移的电子数约为0.2×6.02×1023 |
| C、1 mol乙醇中含有的共价键数约为8×6.02×1023 |
| D、500 mL 1 mol?L-1的硫酸铝溶液中含有的铝离子数为6.02×1023 |
下列离子方程式中正确的是( )
| A、H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、金属钠跟水反应:Na+H2O═Na++OH-+H2↑ |
| C、澄清的石灰水跟盐酸反应:H++OH-═H2O |
| D、氯气与水反应Cl2+H2O?2H++Cl-+ClO- |
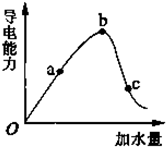 一定温度下,冰醋酸和水稀释过程中溶液的导电能力曲线如图所示,请回答:
一定温度下,冰醋酸和水稀释过程中溶液的导电能力曲线如图所示,请回答: