题目内容
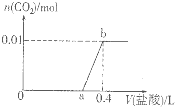 向NaOH和Na2CO3混合溶液中滴加0.1molgL-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是( )
向NaOH和Na2CO3混合溶液中滴加0.1molgL-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是( )| A、在0-a范围内,只发生中和反应 |
| B、ab段发生反应的离子方程式为:CO32-+2H+=CO2↑+H2O |
| C、a=0.2 |
| D、原混合溶液中NaOH与Na2CO3的物质的量之比为2:1 |
考点:有关混合物反应的计算,钠的重要化合物
专题:计算题
分析:对NaOH和Na2CO3混合配成的溶液,当滴加盐酸时,氢氧化钠与盐酸优先发生反应:NaOH+HCl=NaCl+H2O,然后再碳酸钠与盐酸的反应生成碳酸氢钠和氯化钠:HCl+Na2CO3=NaHCO3+NaCl,最后碳酸氢钠与盐酸反应才有二氧化碳气体生成,利用物质的量的关系并结合图象即可解答.
解答:
解:A.向NaOH和Na2CO3混合溶液中滴加盐酸时,首先和NaOH反应生成水和氯化钠:NaOH+HCl=NaCl+H2O,继续滴加时,盐酸和Na2CO3开始反应,首先发生反应HCl+Na2CO3=NaHCO3+NaCl,继续滴加时发生反应:NaHCO3+HCl=NaCl+H2O+CO2↑,此时开始放出气体,故A错误;
B.ab段发生反应为:NaHCO3+HCl=NaCl+H2O+CO2↑,反应的离子方程式为:HCO3-+H+=H2O+CO2↑,故B错误;
C.根据碳元素守恒,混合物中,碳酸钠的物质的量是0.01mol,所以两步反应:HCl+Na2CO3=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,分别消耗的盐酸的量是0.01mol,0.1mol?L-1稀盐酸的体积分别是0.1L,所以a=0.3,故C错误;
D、原混合溶液中NaOH与Na2CO3的物质的量分别是0.02mol和0.01mol,物质的量之比为2:1,故D正确;
故选D.
B.ab段发生反应为:NaHCO3+HCl=NaCl+H2O+CO2↑,反应的离子方程式为:HCO3-+H+=H2O+CO2↑,故B错误;
C.根据碳元素守恒,混合物中,碳酸钠的物质的量是0.01mol,所以两步反应:HCl+Na2CO3=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,分别消耗的盐酸的量是0.01mol,0.1mol?L-1稀盐酸的体积分别是0.1L,所以a=0.3,故C错误;
D、原混合溶液中NaOH与Na2CO3的物质的量分别是0.02mol和0.01mol,物质的量之比为2:1,故D正确;
故选D.
点评:本题考查了混合物反应的计算,题目难度中等,明确碳酸钠与氯化氢反应是分步进行的为解答关键,试题培养了学生分析图象能力及化学计算能力.

练习册系列答案
相关题目
同温同压下,在3支体积不同的试管中分别充满等体积混合的2种气体,它们是:①NO和NO2,②NO2和O2,③NH3和N2.现将3支试管均倒置于水槽中,充分反应后,试管中溶质的物质的量浓度分别为c1、c2、c3(假设溶质全在试管中),则下列关系正确的是( )
| A、c1>c2>c3 |
| B、c1>c3>c2 |
| C、c1=c3>c2 |
| D、c1=c2>c3 |
下列关于有机物的认识正确的是( )
| A、油脂、葡萄糖、蛋白质都是人体重要的营养物质,它们都会水解 |
| B、丁烷(C4H10)和二氯甲烷都存在同分异构体 |
| C、只用新制的Cu(OH)2悬浊液可以鉴别乙酸溶液、葡萄糖溶液和淀粉溶液 |
| D、汽油、柴油、植物油都是碳氢化合物 |
下列物质中,含有自由移动的Cl-的是( )
| A、KCl固体 |
| B、HCl气体 |
| C、KClO3溶液 |
| D、MgCl2溶液 |