题目内容
市场销售的某种食用精制盐包装袋上有如下说明:
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O
(2)上述反应生成的I2可用四氯化碳检验.向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是 .
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体.
以上设计中所缺少的操作在上述步骤中的位置是 ;所缺步骤为 .
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
(2)上述反应生成的I2可用四氯化碳检验.向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体.
以上设计中所缺少的操作在上述步骤中的位置是
考点:氯、溴、碘及其化合物的综合应用,氧化还原反应,氧化还原反应方程式的配平,分液和萃取
专题:
分析:(1)KIO3中I元素的化合价由+5价降低为0,KI中I元素的化合价由-1价升高为0,结合电子守恒及质量守恒定律分析;
(2)①Na2SO3稀溶液与I2反应Na2SO3稀溶液具有还原性被氧化为硫酸钠,I2具有氧化性,被还原为I-,结合反应的电荷守恒和原子守恒配平写出离子方程式;
②Na2SO3稀溶液与碘的四氯化碳溶液不互溶,分层,要使Na2SO3与碘反应,应充分振荡使其接触.
(2)①Na2SO3稀溶液与I2反应Na2SO3稀溶液具有还原性被氧化为硫酸钠,I2具有氧化性,被还原为I-,结合反应的电荷守恒和原子守恒配平写出离子方程式;
②Na2SO3稀溶液与碘的四氯化碳溶液不互溶,分层,要使Na2SO3与碘反应,应充分振荡使其接触.
解答:
解:(1)KIO3中I元素的化合价由+5价降低为0,KI中I元素的化合价由-1价升高为0,由电子守恒及质量守恒定律可知,反应为KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,
故答案为:1、5、3、3、3、3;
(2)①Na2SO3稀溶液与I2反应Na2SO3稀溶液具有还原性被氧化为硫酸钠,I2具有氧化性,被还原为I-,结合反应的电荷守恒和原子守恒配平写出离子方程式,Na2SO3稀溶液与I2反应的离子方程式是:I2+SO32-+H2O=2I-+SO42-+2H+,
故答案为:I2+SO32-+H2O=2I-+SO42-+2H+;
②Na2SO3稀溶液与碘的四氯化碳溶液不互溶,分层,要使Na2SO3与碘反应,应充分振荡使其接触.所以在步骤b后,增加操作:将分液漏斗充分振荡后静置,
故答案为:在步骤b后;将分液漏斗充分振荡后静置.
故答案为:1、5、3、3、3、3;
(2)①Na2SO3稀溶液与I2反应Na2SO3稀溶液具有还原性被氧化为硫酸钠,I2具有氧化性,被还原为I-,结合反应的电荷守恒和原子守恒配平写出离子方程式,Na2SO3稀溶液与I2反应的离子方程式是:I2+SO32-+H2O=2I-+SO42-+2H+,
故答案为:I2+SO32-+H2O=2I-+SO42-+2H+;
②Na2SO3稀溶液与碘的四氯化碳溶液不互溶,分层,要使Na2SO3与碘反应,应充分振荡使其接触.所以在步骤b后,增加操作:将分液漏斗充分振荡后静置,
故答案为:在步骤b后;将分液漏斗充分振荡后静置.
点评:本题综合考查氧化还原反应以及物质的分离提纯,为高频考点,侧重于学生的分析、实验能力的考查,注意把握物质的性质以及相关实验操作,难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
下列实验中,不能达到预期目的是( )
①用升华法分离碘和氯化铵的混合物
②用结晶法分离硝酸钾和氯化钠的混合物
③用分液法分离水和硝基苯的混合物
④用蒸馏法分离乙醇(沸点为78.5℃)和乙酸乙酯(沸点为77.5℃)的混合物.
①用升华法分离碘和氯化铵的混合物
②用结晶法分离硝酸钾和氯化钠的混合物
③用分液法分离水和硝基苯的混合物
④用蒸馏法分离乙醇(沸点为78.5℃)和乙酸乙酯(沸点为77.5℃)的混合物.
| A、①④ | B、②③ | C、③④ | D、②④ |
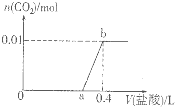 向NaOH和Na2CO3混合溶液中滴加0.1molgL-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是( )
向NaOH和Na2CO3混合溶液中滴加0.1molgL-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是( )| A、在0-a范围内,只发生中和反应 |
| B、ab段发生反应的离子方程式为:CO32-+2H+=CO2↑+H2O |
| C、a=0.2 |
| D、原混合溶液中NaOH与Na2CO3的物质的量之比为2:1 |
a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种.已知由此判断a、b、c、d、e依次为( )
(1)a、c均能与稀硫酸反应放出气体
(2)b与d的硝酸盐反应,置换出单质d
(3)c与强碱反应放出气体,e的一种氧化物具有磁性.
(1)a、c均能与稀硫酸反应放出气体
(2)b与d的硝酸盐反应,置换出单质d
(3)c与强碱反应放出气体,e的一种氧化物具有磁性.
| A、Fe、Cu、Al、Ag、Mg |
| B、Mg、Cu、Al、Ag、Fe |
| C、Al、Cu、Mg、Ag、Fe |
| D、Mg、Ag、Al、Cu、Fe |
下列推断正确的是( )
| 选项 | 事实 | 结论 |
| A | SiO2可用于制光导纤维 | SiO2有导电性 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | Cl2的水溶液可以导电 | Cl2是电解质 |
| D | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
| A、A | B、B | C、C | D、D |
下列叙述中正确的是( )
| A、凡是离子化合物在离子方程式中都要以离子来表示 |
| B、离子互换反应总是向着溶液中离子浓度减小的方向进行 |
| C、酸碱中和反应的实质是H+和OH-结合生成水,故酸碱中和反应的离子方程式都是H++OH-=H2O |
| D、复分解反应必须具备离子反应生成的三个条件才能进行 |
下列离子方程式表达正确的是( )
| A、过氧化钠和水反应:2Na2O2+2H2O=4Na++4OH-+O2↑ |
| B、用铜为电极电解饱和食盐水:2Cl-+2H2O=Cl2↑+H2↑+2OH- |
| C、在明矾溶液中滴加过量氨水:Al3++3OH-=Al(OH)3↓ |
| D、向小苏打溶液中加少量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O |
某可逆反应正向反应过程中能量变化如图所示,下列说法正确的是( )


| A、该反应为吸热反应 |
| B、当反应达到平衡时,降低温度,A的转化率减小 |
| C、升高温度,平衡常数K增大;压强增大,平衡向正反应方向移动 |
| D、加入催化剂,反应速率增大,E1减小,E2减小,反应热不变 |
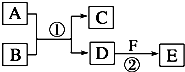 (A、B、C、D、E、F六种物质的转化关系如图(反应条件和部分产物未标出).
(A、B、C、D、E、F六种物质的转化关系如图(反应条件和部分产物未标出).