题目内容
N0为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、1.0L1.0mo1?L-1的NaAlO2水溶液中含有的氧原子数为2N0 |
| B、12g石墨烯(单层石墨)中含有六元环的个数为0.5N0 |
| C、25℃时pH=13的NaOH溶液中含有OH一的数目为0.1 N0 |
| D、1mol的羟基与1 mol的氢氧根离子所含电子数均为9 N0 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.NaAlO2水溶液中,水和偏铝酸钠都含有氧原子;
B.一个六元碳环中含有1×
×6=2个C结合石墨的物质的量计算
C.溶液体积不知不能计算微粒数;
D.依据羟基和氢氧根离子的结构分析判断.
B.一个六元碳环中含有1×
| 1 |
| 3 |
C.溶液体积不知不能计算微粒数;
D.依据羟基和氢氧根离子的结构分析判断.
解答:
解:A.NaAlO2水溶液中,水和偏铝酸钠都含有氧原子,所以1.0L1.0mo1?L-1的NaAlO2水溶液中含有的氧原子数无法计算,故A错误;
B.12g单层石墨的物质的量为1mol,一个六元碳环中含有1×
×6=2个C,所以12g单层石墨中含有六元环的个数为0.5NA,故B正确;
C.溶液体积不知不能计算微粒数,故C错误;
D.1mol的羟基所含电子数为9NA,1mol的氢氧根离子所含电子数为10NA,故D错误;
故选B.
B.12g单层石墨的物质的量为1mol,一个六元碳环中含有1×
| 1 |
| 3 |
C.溶液体积不知不能计算微粒数,故C错误;
D.1mol的羟基所含电子数为9NA,1mol的氢氧根离子所含电子数为10NA,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的分析应用,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意石墨的结构特点.

练习册系列答案
相关题目
在室温下,下列叙述正确的是( )
| A、两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 | ||
| B、Na2CO3溶液加水稀释后,恢复至原温度,pH和KW均减小 | ||
| C、pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等 | ||
D、向0.1 mol?L-1的氨水中加入少量硫酸铵固体,则溶液中
|
在200mL含Mg2+、Al3+、NH4+、H+、Cl-离子的溶液中,逐滴加人4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mo1)的关系如图所示.下列叙述正确的是( )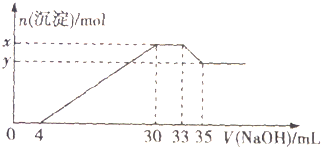

| A、原溶液中n(Mg2+):n(A13+)=10:1 |
| B、原溶液中c(H+)=0.8mol/L |
| C、x与y的差值为0.08 |
| D、原溶液中c(C1-)=0.66mol/L |
在呼吸面具和潜水艇里,过滤空气的最佳物质是( )
| A、NaOH |
| B、Na2O2 |
| C、Na |
| D、Al |
已知:H+(aq)+OH-(aq)═H2O(aq)△H=-57.3kJ/mol,下列说法正确的是( )
| A、NaOH稀溶液分别与稀盐酸和稀醋酸反应生成1 mol H2O,放出热量相同 |
| B、稀盐酸分别与NaOH稀溶液和稀氨水反应生成1 mol H2O,放出热量相同 |
| C、Ba(OH)2稀溶液分别与稀盐酸和稀硫酸反应生成1 mol H2O,放出热量不同 |
| D、该反应说明有水生成的反应是放热反应 |