题目内容
25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)写出次氯酸钠溶液中通入少量二氧化碳的离子方程式 .
(2)常温下0.1mol/L的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是 (填序号).
A.c(H+)B.c(H+)/c(CH3COOH)C.n(H+)D. c(H+)c(CH3COO-)/c(CH3COOH)
(3)体积为10mL c(H+)=10-2mol/L的醋酸溶液与一元酸HX分别加水稀释至1000mL,醋酸溶液与一元酸HX溶液c(H+) 分别为10-5mol/L和10-6mol/L,则HX的电离平衡常数 (填“大于”、“等于”或“小于”)醋酸的电离平衡常数;理由是 .
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平 衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)写出次氯酸钠溶液中通入少量二氧化碳的离子方程式
(2)常温下0.1mol/L的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是
A.c(H+)B.c(H+)/c(CH3COOH)C.n(H+)D. c(H+)c(CH3COO-)/c(CH3COOH)
(3)体积为10mL c(H+)=10-2mol/L的醋酸溶液与一元酸HX分别加水稀释至1000mL,醋酸溶液与一元酸HX溶液c(H+) 分别为10-5mol/L和10-6mol/L,则HX的电离平衡常数
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:(1)电离平衡常数越大,酸的电离程度越大,溶液酸性越强,根据表中数据可知,酸性由强到弱的顺序为:CH3COOH>H2CO3>HClO>HCO3-,据强酸制弱酸书写离子方程式;
(2)CH3COOH溶液加水稀释过程中,醋酸的电离程度增大,氢离子物质的量增大,氢离子浓度、醋酸根离子浓度减小,但氢氧根离子浓度增大;
(3)电离平衡常数越大的弱酸的酸性越强,酸性越弱,加水稀释时电离出的氢离子多,加水稀释时pH变化幅度越小.
(2)CH3COOH溶液加水稀释过程中,醋酸的电离程度增大,氢离子物质的量增大,氢离子浓度、醋酸根离子浓度减小,但氢氧根离子浓度增大;
(3)电离平衡常数越大的弱酸的酸性越强,酸性越弱,加水稀释时电离出的氢离子多,加水稀释时pH变化幅度越小.
解答:
解:(1)据酸性由强到弱的顺序:CH3COOH>H2CO3>HClO>HCO3-,次氯酸钠溶液中通入少量二氧化碳应该生成次氯酸和碳酸氢钠,离子方程式为:ClO-+H2O+CO2=HClO+HCO3-,故答案为:ClO-+H2O+CO2=HClO+HCO3-;
(2)A、0.1mol?L-1的CH3COOH溶液加稀释过程中,溶液中氢离子浓度减小,故A正确;
B、0.1mol?L-1的CH3COOH溶液加稀释过程中,各个微粒浓度减小,同时醋酸的电离向右移动,c(H+)减小的程度小于c(CH3COOH)的减小程度,所以
增大,故B错误;
C、CH3COOH溶液加水稀释过程中,醋酸的电离程度增大,氢离子物质的量增大,故C错误;
D、
为醋酸的电离平衡常数,由于温度不变,则水的电离平衡常数不变,故D错误;
故答案为:A;
(3)电离平衡常数越大,对应弱酸的酸性越强,酸性越弱,加水稀释时电离出的氢离子多,加水稀释时pH变化幅度越小,加水稀释相同倍数,HA的pH变化大,说明HA的酸性比醋酸强,故答案为:大于;酸性越弱,加水稀释时电离出的氢离子多,加水稀释时pH变化幅度越小.
(2)A、0.1mol?L-1的CH3COOH溶液加稀释过程中,溶液中氢离子浓度减小,故A正确;
B、0.1mol?L-1的CH3COOH溶液加稀释过程中,各个微粒浓度减小,同时醋酸的电离向右移动,c(H+)减小的程度小于c(CH3COOH)的减小程度,所以
| c(H+) |
| c(CH3COOH) |
C、CH3COOH溶液加水稀释过程中,醋酸的电离程度增大,氢离子物质的量增大,故C错误;
D、
| c(H+)?c(CH3COO-) |
| c(CH3COOH) |
故答案为:A;
(3)电离平衡常数越大,对应弱酸的酸性越强,酸性越弱,加水稀释时电离出的氢离子多,加水稀释时pH变化幅度越小,加水稀释相同倍数,HA的pH变化大,说明HA的酸性比醋酸强,故答案为:大于;酸性越弱,加水稀释时电离出的氢离子多,加水稀释时pH变化幅度越小.
点评:本题考查了电离平衡常数和酸性强弱的关系、弱酸加水稀释时各离子浓度的变化以及pH变化与酸性强弱的关系,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
N0为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、1.0L1.0mo1?L-1的NaAlO2水溶液中含有的氧原子数为2N0 |
| B、12g石墨烯(单层石墨)中含有六元环的个数为0.5N0 |
| C、25℃时pH=13的NaOH溶液中含有OH一的数目为0.1 N0 |
| D、1mol的羟基与1 mol的氢氧根离子所含电子数均为9 N0 |
“纳米技术”广泛地应用于催化及军事科学中,“纳米材料”是指粒子直径在几纳米到几十纳米(nm)之间的材料(1nm=10-9m).如将纳米材料分散到液体分散剂中,所得混合物具有的性质是( )
| A、能全部透过半透膜 |
| B、用激光笔照射有光亮的“通路” |
| C、所得溶液一定能导电 |
| D、所得物质一定为悬浊液或乳浊液 |
有机物X、Y分子式不同,它们只含C、H、O元素中的两种或三种,若将X、Y不论何种比例混合,只要其物质的量之和不变,完全燃烧时耗氧气量也不变.X、Y可能是( )
| A、CH4、C2H4O2 |
| B、C2H2、C6H6 |
| C、CH2O、C3H6O2 |
| D、C2H4、C2H6 |
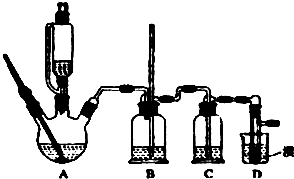
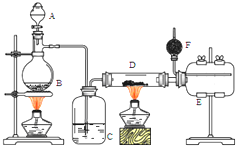 无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾.实验室用如下装置制备少量无水氯化铝,其反应原理为:2Al+6HCl(g)═2AlCl3+3H2.完成下列填空:
无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾.实验室用如下装置制备少量无水氯化铝,其反应原理为:2Al+6HCl(g)═2AlCl3+3H2.完成下列填空: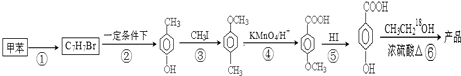
 在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式)
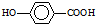
在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式) 的同分异构体很多,其中符合下列条件有
的同分异构体很多,其中符合下列条件有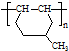 是一种建筑材料,根据题中合成路线信息,以甲苯为原料合成该高分子化合物,请设计合成路线(无机试剂及溶剂任选).注:合成路线的书写格式参照如下示例流程图:
是一种建筑材料,根据题中合成路线信息,以甲苯为原料合成该高分子化合物,请设计合成路线(无机试剂及溶剂任选).注:合成路线的书写格式参照如下示例流程图:

 实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH