题目内容
1.有4.8g CuO、Fe2O3组成的混合物与充足的CO于加热条件下充分反应,得到m g固体,反应后全部气体用0.6mol•L-1 Ba(OH)2溶液100mL处理,有白色沉淀生成,又知反应后生成的气体质量为3.52g.下列有关说法正确的是( )| A. | 将得到的m g固体放到氧气中充分灼烧后,固体质量变为4.8 g | |
| B. | 生成的CO2已被Ba(OH)2溶液完全吸收,Ba2+沉淀完全 | |
| C. | Ba(OH)2溶液吸收CO2后的溶液中有BaCO3和Ba(HCO3)2,且物质的量的比为2:1 | |
| D. | 原混合物中CuO与Fe2O3的质量比为2:1 |
分析 CuO、Fe2O3混合物跟足量CO充分反应生成Cu、Fe单质及CO2,反应后生成3.52g气体为二氧化碳,物质的量为:$\frac{3.52g}{44g/mol}$=0.08mol,金属氧化物中的氧元素的物质的量与二氧化碳的物质的量相等,则原混合物中含有氧原子的物质的量为0.8mol,设混合物中CuO、Fe2O3的物质的量分别为xmol、ymol,则:x+3y=0.8mol、80x+160y=4.8,联立解得:x=0.02、y=0.02,故原混合物中CuO与Fe2O3物质的量的都为0.02mol;
CuO、Fe2O3混合物跟足量CO充分反应;
n[Ba(OH)2]=0.6mol/L×0.1L=0.06mol,故n(CO2):n[Ba(OH)2]=0.08mol:0.06mol=4:3,介于1:1与2:1之间,故生成碳酸钡与碳酸氢钡;设出碳酸钡与碳酸氢钡物质的量分别为amol、bmol,根据钡离子守恒、碳元素守恒列方程计算,据此进行解答.
解答 解:CuO、Fe2O3混合物跟足量CO充分反应生成Cu、Fe单质及CO2,反应后生成3.52g气体为二氧化碳,物质的量为:$\frac{3.52g}{44g/mol}$=0.08mol,金属氧化物中的氧元素的物质的量与二氧化碳的物质的量相等,则原混合物中含有氧原子的物质的量为0.8mol,设混合物中CuO、Fe2O3的物质的量分别为xmol、ymol,则:x+3y=0.8mol、80x+160y=4.8,联立解得:x=0.02、y=0.02,故原混合物中CuO与Fe2O3物质的量的都为0.02mol,
A.将得到的m g固体放到氧气中充分灼烧后得到的产物为CuO、Fe3O4,所得固体的质量增大,故A错误;
B.n[Ba(OH)2]=0.6mol/L×0.1L=0.06mol,故n(CO2):n[Ba(OH)2]=0.08mol:0.06mol=4:3,介于1:1与2:1之间,故生成碳酸钡与碳酸氢钡,故B错误;
C.根据B可知,氢氧化钡与二氧化碳反应生成了碳酸钡和碳酸氢钡的混合物,碳酸钡与碳酸氢钡物质的量分别为amol、bmol,根据钡离子守恒、碳元素守恒可得:a+2b=0.08、a+b=0.06,解得:a=0.04、b=0.02,则生成碳酸钡与碳酸氢钡的物质的量之比为0.04mol:0.02mol=2:1,故C正确;
D.原混合物中CuO、Fe2O3的质量之比为80g/mol×0.02mol:160g/mol×0.02mol=1:2,故D错误;
故选C.
点评 本题考查混合物的有关计算,题目难度中等,明确反应反应的实质为解答关键,利用守恒思想在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案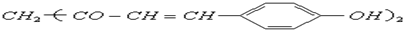 ,用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )
,用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )| A. | 3mol 3mol | B. | 3mol 5mol | C. | 6 mol 10 mol | D. | 6 mol 8 mol |
| Y | V | |||
| X | W |
| A. | 原子半径:X>W>V>Y | |
| B. | Y的最高价氧化物的电子式为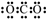 | |
| C. | X的最高价氧化物能与V、W最高价氧化物对应的水化物反应 | |
| D. | 甲、乙混合时所生成的物质为离子化合物,既含有离子键又含有非极性键 |
| A. | 生石灰和水的反应 | B. | 木炭在氧气中燃烧 | ||
| C. | 石灰石在高温下的分解反应 | D. | 盐酸与氢氧化钠溶液的反应 |
| … | E | A | B | ||
| C | … | D |
(2)A与B可组成质量比为7:16的三原子分子,该分子与水反应的化学方程式:3NO2+H2O=2HNO3+NO;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若所得溶液的pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
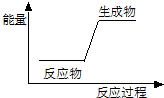
(5)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g)与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
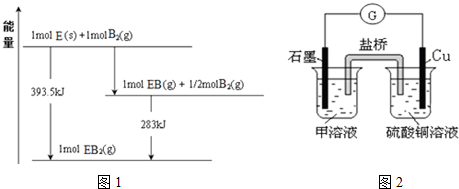
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将某气体通入FeCl2溶液中 | 溶液由浅绿色变为黄色 | 该气体中一定含有Cl2 |
| B | 将某气体通入品红溶液中 | 品红溶液褪色 | 该气体中一定含有SO2 |
| C | 将某气体通过灼热的CuO粉末 | 粉末由黑变红 | 该气体中一定含有H2 |
| D | 将某气体与湿润的红色石蕊试纸接触 | 试纸变蓝色 | 该气体中一定含有NH3 |
| A. | A | B. | B | C. | C | D. | D |
| A. | KClO3在反应中得到电子 | |
| B. | ClO2是氧化产物 | |
| C. | H2C2O4在反应中被氧化 | |
| D. | 1 mol KClO3参加反应,有2 mol电子转移 |