题目内容
14.X、Y、Z、M是组成蛋白质最主要的元素,其原子序数依次增大.(1)Y在元素周期表中的位置是第二周期IVA族.
(2)Z元素的原子结构示意图是
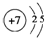 .
.(3)X与Z组成的离子化合物ZX5,其电子式是
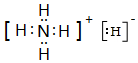 .
.(4)常温下,pH=2的甲(强酸)、1mol/LpH=12的乙(碱)都是由X、Y、Z、M中的三种元素组成,两物质等体积混合后,各离子浓度大小顺序为c(NH4+)>c(NO3-)>c(OH-)>c(H+);.
(5)液体Y2X8Z2与液体Z2M4反应可以为火箭升入太空提供巨大的能量,其发生的化学方程式是C2H8N2+2N2O4=2CO2+3N2+4H2O.
分析 X、Y、Z、M四种元素是组成蛋白质的基础元素,它们的原子序数依次增大,则X为H元素,Y为C元素,Z为N元素,M为O元素.
(1)周期数=电子层数、主族族序数=最外层电子数;
(2)Z为N元素,核外电子数为7,有2个电子层,个电子数为2、5;
(3)X与Z组成的离子化合物ZX5为NH4H,由铵根离子与氢负离子构成;
(4)常温下,pH=2的甲(强酸)、1mol/LpH=12的乙(碱)都是由H、C、N、O中的三种元素组成,则甲为HNO3,乙为NH3.H2O,两物质等体积混合后,为NH4NO3、NH3.H2O混合溶液,且NH3.H2O的浓度远远大于NH4NO3的浓度,NH3.H2O的电离程度大于铵根离子的水解程度,溶液呈碱性;
(5)液体C2H8N2与液体N2O4反应可以为火箭升入太空提供巨大的能量,反应生成氮气、二氧化碳与水.
解答 X、Y、Z、M四种元素是组成蛋白质的基础元素,它们的原子序数依次增大,则X为H元素,Y为C元素,Z为N元素,M为O元素.
(1)Y为碳元素,原子核外有2个电子层,最外层电子数为4,处于元素周期表中第二周期IVA族,
故答案为:第二周期IVA族;
(2)Z为N元素,核外电子数为7,有2个电子层,个电子数为2、5,原子结构示意图为: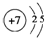 ,
,
故答案为: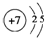 ;
;
(3)X与Z组成的离子化合物ZX5为NH4H,由铵根离子与氢负离子构成,其电子式为: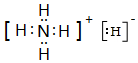 ,
,
故答案为: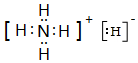 ;
;
(4)常温下,pH=2的甲(强酸)、1mol/LpH=12的乙(碱)都是由H、C、N、O中的三种元素组成,则甲为HNO3,乙为NH3.H2O,两物质等体积混合后,为NH4NO3、NH3.H2O混合溶液,且NH3.H2O的浓度远远大于NH4NO3的浓度,NH3.H2O的电离程度大于铵根离子的水解程度,溶液呈碱性,溶液中铵根离子浓度大于硝酸根的,溶液中离子浓度顺序为:c(NH4+)>c(NO3-)>c(OH-)>c(H+),
故答案为:c(NH4+)>c(NO3-)>c(OH-)>c(H+);
(5)液体C2H8N2与液体N2O4反应可以为火箭升入太空提供巨大的能量,反应生成氮气、二氧化碳与水,化学反应方程式为:C2H8N2+2N2O4=2CO2+3N2+4H2O,
故答案为:C2H8N2+2N2O4=2CO2+3N2+4H2O.
点评 本题以蛋白质组成元素为载体,考查核外电子排布、电子式、盐类水解、陌生方程式书写等,题目培养学生知识迁移运用能力,难度不大,注意对基础知识的理解掌握.

| A. | 氯化钙的化学式 CaCl2 | B. | HCl分子的电子式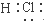 | ||
| C. | 氯化钠的电子式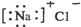 | D. | 氯原子的结构示意图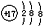 |
| A. | 固体悬浮微粒是造成雾霾天气的一种重要因素 | |
| B. | 一氧化碳、氮氧化物是酸雨形成的主要因素 | |
| C. | 含铅化合物导致人体蛋白质变性是物理变化 | |
| D. | 汽车尾气可通过净化装置将碳氢化合物还原成CO2和H2O |
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Al | P | S | Cl |
(2)氧的原子结构示意图是
 ;
;(3)形成化合物种类最多的元素是C;
(4)HF和H2O中,热稳定性较强的是HF;
(5)N和P中,原子半径较小的是N;
(6)常温下,会在浓硫酸中发生钝化的金属是Al;
(7)元素最高价氧化物对应水化物中,碱性最强的是NaOH(填化学式),酸性最强的是HClO4(填“H2SO4”或“HClO4”).
| A. | 将经过无害化处理的生活污水排放到漓江中 | |
| B. | 漓江沿岸不得开设造纸厂等污染企业 | |
| C. | 定期投放水生动物优化漓江生态 | |
| D. | 使用含磷洗涤剂且将洗涤后的废水排放到漓江中 |
| A. | 二溴乙烷 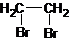 | B. | 3-乙基-1-丁烯 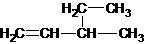 | ||
| C. | 2-甲基-2,4-己二烯 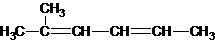 | D. | 2,2,3-三甲基戊烷 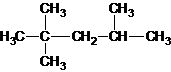 |
 .
.