题目内容
2.如表是元素周期表的一部分,根据表中给出的10种元素,回答下列问题.| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Al | P | S | Cl |
(2)氧的原子结构示意图是
 ;
;(3)形成化合物种类最多的元素是C;
(4)HF和H2O中,热稳定性较强的是HF;
(5)N和P中,原子半径较小的是N;
(6)常温下,会在浓硫酸中发生钝化的金属是Al;
(7)元素最高价氧化物对应水化物中,碱性最强的是NaOH(填化学式),酸性最强的是HClO4(填“H2SO4”或“HClO4”).
分析 (1)稀有气体的性质最不活泼;
(2)O的质子数为8;
(3)C元素形成的有机物化合物种类最多;
(4)非金属性越强,对应氢化物越稳定;
(5)电子层越多,原子半径越大;
(6)常温下,Fe或Al遇浓硫酸发生钝化;
(7)元素最高价氧化物对应水化物中,高氯酸的酸性最强,氢氧化钠的碱性最强.
解答 解:(1)稀有气体的性质最不活泼,则单质的化学性质最不活沷的元素是Ne,故答案为:Ne;
(2)O的质子数为8,则氧的原子结构示意图为 ,故答案为:
,故答案为: ;
;
(3)形成化合物种类最多的元素是C,故答案为:C;
(4)非金属性F>O,HF和H2O中,热稳定性较强的是HF,故答案为:HF;
(5)电子层越多,原子半径越大,则N和P中,原子半径较小的是N,故答案为:N;
(6)常温下,会在浓硫酸中发生钝化的金属是Al,故答案为:Al;
(7)元素最高价氧化物对应水化物中,碱性最强的是NaOH,酸性最强的是HClO4,故答案为:NaOH;HClO4.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置和性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
7.有些化学反应不仅与反应物种类有关,还与反应条件(反应温度、反应物浓度)或反应物物质的量的比值有关,下列反应中不随反应条件(反应温度、反应物浓度)、反应物物质的量的而变化的是( )
| A. | 氯气与铁粉 | B. | 二氧化碳与石灰水 | ||
| C. | 锌与硫酸 | D. | 碳酸钠与硫酸 |
8.下列说法正确的是( )
| A. | 只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 | |
| B. | 将NH4Cl溶液蒸干制备NH4Cl固体 | |
| C. | 因为NH3能使酚酞溶液变红,NH3用于设计喷泉实验 | |
| D. | 浓氨水可检验氯气管道是否漏气 |
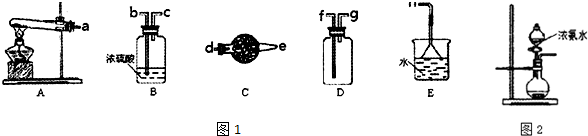
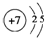 .
. .
.