��Ŀ����
W��X��Y��Z��M��Q��Ϊ��ϡ��������Ķ�����Ԫ�أ���ԭ��������������X��������������W��4����Z��M��������ϼ���ͬ��X��M�����ڱ���λ�������ʾ��
��1��X�����ڱ��е�λ��Ϊ ��Q��Ԫ������Ϊ ��
��2��Z��W�γɵ�4�����ӵĵ���ʽΪ ��
��3����W��Y��Z��M��ɵ����ӻ���������Һ�����Ӧ�����ӷ���ʽΪ ��
��4��W2��Z2��Ӧ������ף�W2��Q2��Ӧ���ɻ������ң���֪��Ӧ���ң�g��+Z2��g�����ף�g��+Q2��g����ÿ����1mol Q2����57.8kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ ��
��5��X��Y�ɷֱ���Z��ԭ�Ӹ�����1��1�γɻ�������Ͷ����ڴ������������£����붡�������淴Ӧ�����ɵ���Y2����һ�ֻ������죮д���÷�Ӧ�Ļ�ѧ����ʽ ��
��6����1mol�������1mol���������һװ�д����ĺ�ѹ�����У���ַ�Ӧ��ƽ���
�������������ԭ������23%����ת����Ϊ ��
����֪�÷�Ӧ��H��0���������¶ȣ�ƽ�ⳣ��Kֵ�� ������С�䣩��
��������ѹǿ����Ϊԭ����2�����ٴδ�ƽ���������ж������������ ������С�䣩��
| X | ||
| M |
��2��Z��W�γɵ�4�����ӵĵ���ʽΪ
��3����W��Y��Z��M��ɵ����ӻ���������Һ�����Ӧ�����ӷ���ʽΪ
��4��W2��Z2��Ӧ������ף�W2��Q2��Ӧ���ɻ������ң���֪��Ӧ���ң�g��+Z2��g�����ף�g��+Q2��g����ÿ����1mol Q2����57.8kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ
��5��X��Y�ɷֱ���Z��ԭ�Ӹ�����1��1�γɻ�������Ͷ����ڴ������������£����붡�������淴Ӧ�����ɵ���Y2����һ�ֻ������죮д���÷�Ӧ�Ļ�ѧ����ʽ
��6����1mol�������1mol���������һװ�д����ĺ�ѹ�����У���ַ�Ӧ��ƽ���
�������������ԭ������23%����ת����Ϊ
����֪�÷�Ӧ��H��0���������¶ȣ�ƽ�ⳣ��Kֵ��
��������ѹǿ����Ϊԭ����2�����ٴδ�ƽ���������ж������������
���㣺Ԫ�������ɺ�Ԫ�����ڱ����ۺ�Ӧ��
ר�⣺Ԫ����������Ԫ�����ڱ�ר��
������W��X��Y��Z��M��Q��Ϊ��ϡ��������Ķ�����Ԫ�أ���ԭ��������������X��������������W��4����Z��M��������ϼ���ͬ����Z��Mλ��ͬһ���壬����Ԫ�������ڱ��е�λ��֪��Xλ�ڵڶ����ڣ�Mλ�ڵ������ڣ�����������������8����W������������1����ԭ��������С��ΪLi��HԪ�ء�XΪCԪ�أ�M��SԪ�أ�Z��Mλ��ͬһ���壬��Z��OԪ�أ�Y��NԪ�أ�QΪClԪ�أ�Z��W�γɵ�4�����ӣ���W��HԪ�أ�������ʽṹ���ʽ��ǰ��С�⣻
��4�������Ȼ�ѧ����ʽ���������ش�
��5�����������֪��Ϣ��д��ѧ��Ӧ����ʽ��
��6�����������ʵ��������������֪���ݽ��м��㼴�ɣ�
��4�������Ȼ�ѧ����ʽ���������ش�
��5�����������֪��Ϣ��д��ѧ��Ӧ����ʽ��
��6�����������ʵ��������������֪���ݽ��м��㼴�ɣ�
���
�⣺W��X��Y��Z��M��Q��Ϊ��ϡ��������Ķ�����Ԫ�أ���ԭ��������������X��������������W��4����Z��M��������ϼ���ͬ����Z��Mλ��ͬһ���壬����Ԫ�������ڱ��е�λ��֪��Xλ�ڵڶ����ڣ�Mλ�ڵ������ڣ�����������������8����W������������1����ԭ��������С��ΪLi��HԪ�ء�XΪCԪ�أ�M��SԪ�أ�Z��Mλ��ͬһ���壬��Z��OԪ�أ�Y��NԪ�أ�QΪClԪ�أ�Z��W�γɵ�4�����ӣ���W��HԪ�أ�
��1��X��CԪ�أ�λ�ڵڶ����ڵ�IVA�壬Q����Ԫ�أ��ʴ�Ϊ���ڶ����ڡ�IVA�壻�ȣ�
��2��Z��W�γɵ�4������Ϊˮ�������ӣ������ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3����W��Y��Z��M��ɵ����ӻ����������������ƺ��������ƣ�����������Һ��ǿ���ԣ������Ӻ�������������ӷ�Ӧ���ɶ��������ˮ����Ӧ����ʽΪ��SO32-+2H+=SO2��+H2O �� HSO3-+H+=SO2��+H2O��
�ʴ�Ϊ��SO32-+2H+=SO2��+H2O �� HSO3-+H+=SO2��+H2O��
��4��H2��O2��Ӧ���ɻ������ΪH2O��H2��Cl2��Ӧ���ɻ�������ΪHCl����֪��HCl��g��+O2��g����H2O��g��+Cl2��g����ÿ����1mol Cl2����57.8kJ����÷�Ӧ���Ȼ�ѧ����ʽΪ��2HCl��g��+
O2��g��=H2O��g��+Cl2��g����H=-57.8 kJ/mo��4HCl��g��+O2��g��=2H2O��g�� 2Cl2��g����H=-115.6 kJ/mol��
�ʴ�Ϊ��2HCl��g��+
O2��g��=H2O��g��+Cl2��g����H=-57.8 kJ/mo��4HCl��g��+O2��g��=2H2O��g�� 2Cl2��g����H=-115.6 kJ/mol��
��5��C��N�ɷֱ���O��ԭ�Ӹ�����1��1�γɻ�������Ͷ������ΪCO����ΪNO���ڴ������������£����붡�������淴Ӧ�����ɵ���N2����һ�ֻ������죬����Ԫ���غ㼰����ת���غ��֪��ΪCO2���÷�Ӧ�Ļ�ѧ����ʽ��2CO+2NO N2+2CO2���ʴ�Ϊ��2CO+2NO
N2+2CO2���ʴ�Ϊ��2CO+2NO N2+2CO2��
N2+2CO2��
��6����1molCO�����1molNO�������һװ�д����ĺ�ѹ�����У���ַ�Ӧ��ƽ���
�������������ԭ������23%����������������ʵ���=��1mol+1mol����23%=0.46mol����
2CO+2NO N2+2CO2 �������ʵ�������
N2+2CO2 �������ʵ�������
2 1
n��NO�� 0.46mol
��n��NO��=
=0.92mol��
��NO��ת����=
��100%=92%��
�ʴ�Ϊ��92%��
�ڶ��ڷ��ȷ�Ӧ���¶����ߣ���K��С���ʴ�Ϊ����С��
������ѹǿ����ѧƽ�������ƶ��������ٴδ�ƽ����������NO�������������С���ʴ�Ϊ����С��
��1��X��CԪ�أ�λ�ڵڶ����ڵ�IVA�壬Q����Ԫ�أ��ʴ�Ϊ���ڶ����ڡ�IVA�壻�ȣ�
��2��Z��W�γɵ�4������Ϊˮ�������ӣ������ʽΪ
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
����3����W��Y��Z��M��ɵ����ӻ����������������ƺ��������ƣ�����������Һ��ǿ���ԣ������Ӻ�������������ӷ�Ӧ���ɶ��������ˮ����Ӧ����ʽΪ��SO32-+2H+=SO2��+H2O �� HSO3-+H+=SO2��+H2O��
�ʴ�Ϊ��SO32-+2H+=SO2��+H2O �� HSO3-+H+=SO2��+H2O��
��4��H2��O2��Ӧ���ɻ������ΪH2O��H2��Cl2��Ӧ���ɻ�������ΪHCl����֪��HCl��g��+O2��g����H2O��g��+Cl2��g����ÿ����1mol Cl2����57.8kJ����÷�Ӧ���Ȼ�ѧ����ʽΪ��2HCl��g��+
| 1 |
| 2 |
�ʴ�Ϊ��2HCl��g��+
| 1 |
| 2 |
��5��C��N�ɷֱ���O��ԭ�Ӹ�����1��1�γɻ�������Ͷ������ΪCO����ΪNO���ڴ������������£����붡�������淴Ӧ�����ɵ���N2����һ�ֻ������죬����Ԫ���غ㼰����ת���غ��֪��ΪCO2���÷�Ӧ�Ļ�ѧ����ʽ��2CO+2NO
 N2+2CO2���ʴ�Ϊ��2CO+2NO
N2+2CO2���ʴ�Ϊ��2CO+2NO N2+2CO2��
N2+2CO2����6����1molCO�����1molNO�������һװ�д����ĺ�ѹ�����У���ַ�Ӧ��ƽ���
�������������ԭ������23%����������������ʵ���=��1mol+1mol����23%=0.46mol����
2CO+2NO
 N2+2CO2 �������ʵ�������
N2+2CO2 �������ʵ�������2 1
n��NO�� 0.46mol
��n��NO��=
| 0.46��2 |
| 1 |
��NO��ת����=
| 0.92 |
| 1 |
�ʴ�Ϊ��92%��
�ڶ��ڷ��ȷ�Ӧ���¶����ߣ���K��С���ʴ�Ϊ����С��
������ѹǿ����ѧƽ�������ƶ��������ٴδ�ƽ����������NO�������������С���ʴ�Ϊ����С��
���������⿼����Ԫ�������ɺ�Ԫ�����ڱ����ۺ�Ӧ�ã��漰�Ȼ�ѧ����ʽ����д����ѧƽ����ƶ��Լ������֪ʶ�㣬����ԭ�ӽṹ���Ԫ����������������������ۺ�֪ʶ�Ŀ��飬�ѶȽϴ�

��ϰ��ϵ�д�
 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д� �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
�����Ŀ
���й������漰��ѧ�仯��������������ԭ��Ӧ���ǣ�������
| A����ͥ�о�����ʳ������ˮ����ˮ�� |
| B����ɫ��Ӧ�����Ȼ��ƺ��Ȼ�����Һ |
| C���ձ������˵�վ�˷�Ӧ����U-235�ѱ�����-133���-135 |
| D����ͨ�����������ظ���ؼ��˾���Ƿ�ƺ�ݳ� |
һ���¶��£����������ܱ������н������п��淴Ӧ��N2+3H2?2NH3�����ж����и������˵���÷�Ӧ�Ѿ��ﵽ��ѧƽ��״̬���ǣ�������
| A����Ӧ��Ũ�ȵ���������Ũ�� |
| B��������N2��H2��NH3Ũ��֮��Ϊ1��3��2 |
| C��3v��N2����=v��H2���� |
| D����Ӧ�����ϵ��ѹǿ����ʱ��ı仯���仯 |
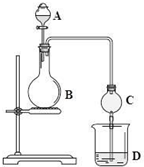 ��ѧʵ���У�ͬһ��װ�ÿ������ڲ�ͬ��ʵ�飬����ͼ�е�ʵ��װ�ã�����ͼ��ʾ��B�п�Ϊ�����Һ�壬�ɼ��ȣ�
��ѧʵ���У�ͬһ��װ�ÿ������ڲ�ͬ��ʵ�飬����ͼ�е�ʵ��װ�ã�����ͼ��ʾ��B�п�Ϊ�����Һ�壬�ɼ��ȣ� ��1����֪25��ʱ��C2H5OH��l����ȼ����Ϊ1366.8kJ/mol�����Ȼ�ѧ����ʽ��ʾ��
��1����֪25��ʱ��C2H5OH��l����ȼ����Ϊ1366.8kJ/mol�����Ȼ�ѧ����ʽ��ʾ��