题目内容
3.C1O2是一种常用的气体消毒剂,能净化有毒废水中的NaCN (已知NaCN中N的化合价为-3),发生的反应为:2C1O2+2NaCN═2NaCl+2CO2+N2,下列说法正确的是( )| A. | 反应中氯元素被氧化 | |
| B. | NaCN既是氧化剂又是还原剂 | |
| C. | 生成0.lmol N2,转移1mol电子 | |
| D. | 氧化产物与还原产物的物质的域之比为1:1 |
分析 反应2C1O2+2NaCN═2NaCl+2CO2+N2中,Cl元素的化合价由+4降低为-1价,N元素的化合价由-3价升高为0,C元素的化合价由+2价升高为+4价,该反应中转移10e-,以此解答.
解答 解:A.C、N元素化合价都升高,Cl元素的化合价降低,则反应中氯元素被还原,故A错误;
B.NaCN中C、N元素化合价都升高,只是还原剂,故B错误;
C.该反应中转移10e-,则生成0.lmol N2,转移1mol电子,故C正确;
D.反应中CO2和N2是氧化产物,C1O2是还原产物,则氧化产物与还原产物的物质的量之比为3:2,故D错误.
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化及氧化还原反应中规律性知识为解答的关键,题目难度不大,侧重于考查学生的分析能力和应用能力.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
13.下列热化学方程式书写错误的是( )
| A. | C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol | B. | 2SO2(g)+O2(g)=SO3(g)△H=-196.6kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol | D. | 2H2(g)+O2(g)=2H2O(l)△H=-517.6kJ/mol |
11.下列与化学概念有关的说法正确的是( )
| A. | Na2O、CaO、Al2O3均为碱性氧化物 | |
| B. | 水玻璃、漂白液、液氯均为混合物 | |
| C. | 氨水能够导电,所以氨水是电解质 | |
| D. | 有单质参加或生成的化学反应不一定是氧化还原反应 |
18.下列实验操作或装置(略去部分夹持仪器)正确的是( )
| A. | 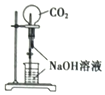 喷泉实验 | B. |  配制一定物质的量浓度的NaCl溶液 | ||
| C. | 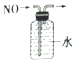 排水法收集NO | D. |  碳酸氢钠受热分解 |
8.下列反应的离子方程式书写正确的是( )
| A. | 钠和硫酸铜溶液反应:2Na+Cu2+═Cu2+2Na+ | |
| B. | 工业上将Cl2通入石灰乳中制漂白粉:Cl2+2OH-═Cl-+ClO-+H2O | |
| C. | 向Ba(OH)2溶液中加入少量的NH4HSO4溶液:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 1.0mol/L的NaAlO2溶液和2.5mol/L的盐酸等体积混合2AlO2-+5H+═Al3++Al(OH)3↓+H2O |
12.下列行为符合安全要求的是( )
| A. | 实验室制取氨气时,将尾气直接通入水中吸收 | |
| B. | 金属钠着火,立即用泡沫灭火器灭火 | |
| C. | 大量氯气泄漏时,迅速离开现场并尽量往高处去 | |
| D. | 皮肤上不慎沾上浓NaOH溶液,立即用盐酸冲洗 |
13.下列防止钢铁锈蚀的措施不合理的是 ( )
| A. | 在自行车的钢圈表面镀镍 | B. | 在地下钢铁管道上连接铜块 | ||
| C. | 改变金属内部结构制成不锈钢 | D. | 健身器村刷油漆或包上一层塑料层 |
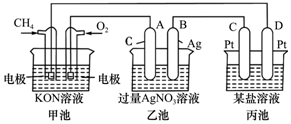 根据下列电化学装置,回答下列问题:
根据下列电化学装置,回答下列问题: