题目内容
2.除去下列杂质(括号内是杂质)所用试剂不正确的是( )| A. | CO2(HCl):用饱和NaHCO3溶液 | B. | CO2(SO2):用饱和KMnO4溶液 | ||
| C. | Cl2(HCl):用饱和NaCl溶液 | D. | SO2(HCl):用饱和NaOH溶液 |
分析 A.HCl与饱和碳酸氢钠反应生成二氧化碳;
B.SO2与高锰酸钾发生氧化还原反应,而CO2不能;
C.HCl极易溶于水,食盐水抑制氯气的溶解;
D.二者均与NaOH溶液反应.
解答 解:A.HCl与饱和碳酸氢钠反应生成二氧化碳,则洗气可除杂,故A正确;
B.SO2与高锰酸钾发生氧化还原反应,而CO2不能,则洗气可除杂,故B正确;
C.HCl极易溶于水,食盐水抑制氯气的溶解,则洗气可除杂,故C正确;
D.二者均与NaOH溶液反应,不能除杂,应选饱和亚硫酸氢钠、洗气除杂,故D错误;
故选D.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质与性质差异为解答的关键,侧重分析与应用能力考查,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
相关题目
12.下列实验设计不能达到实验目的是( )
| 选项 | 实验设计 | 实验目的 |
| A | 过氧化钠与水反应 | 制备少量干燥的氧气 |
| B | 取铁在氧气中充分燃烧后的固体产物溶于稀硫酸,加KSCN溶液 | 检验铁的燃烧产物中含+3价铁 |
| C | 分别取大小相近的钠粒、钾粒投入水中,观察反应的剧烈程度 | 比较钠、钾的还原性强弱 |
| D | 将CO2气体通入Na2SiO3溶液中 | 比较C、Si元素非金属性的强弱 |
| A. | A | B. | B | C. | C | D. | D |
13.某元素原子最外层上只有两个电子,该元素( )
| A. | 一定是金属元素 | |
| B. | 一定能和氢氧化钠溶液反应生成氢气 | |
| C. | 一定是ⅡA族元素 | |
| D. | 可能是金属元素,也可能不是金属元素 |
10.向KI、Na2S2O3、淀粉三种物质按一定比例组成的混合溶液中快速加入一定量的(NH4)2S2O8溶液并开始计时,ts时观察到溶液变蓝色,过程中发生下列反应:①2I-+S2O82-=I2+2SO42-(慢),②I2+2S2O32-=2I-+S4O62- (快)下列说法正确的是( )
| A. | 总反应速率由反应②决定 | |
| B. | 在(NH4)2S2O8消耗完后,溶液一定显蓝色 | |
| C. | 若能观察都蓝色出现,刚起始时,n(Na2S2O3)=n[(NH4)2S2O8] | |
| D. | 升高温度,①、②的反应速率均加快 |
17. 某无色稀溶液X中,可能含有下表所列离子中的某几种.
某无色稀溶液X中,可能含有下表所列离子中的某几种.
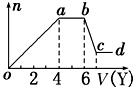
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示.
(1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是AlO2-、SiO32-,ab段发生反应的离子是CO32-,bc段发生反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
(2)若Y是NaOH溶液,则X中一定含有的阳离子是Al3+、Mg2+、NH4+,其物质的量之比为2:1:4,ab段反应的离子方程式为NH4++OH-═NH3•H2O.
 某无色稀溶液X中,可能含有下表所列离子中的某几种.
某无色稀溶液X中,可能含有下表所列离子中的某几种.| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
(1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是AlO2-、SiO32-,ab段发生反应的离子是CO32-,bc段发生反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
(2)若Y是NaOH溶液,则X中一定含有的阳离子是Al3+、Mg2+、NH4+,其物质的量之比为2:1:4,ab段反应的离子方程式为NH4++OH-═NH3•H2O.
7.在K2Cr2O7溶液中存在下列平衡:2CrO42- (黄色)+2H+?Cr2O72- (橙色)+H2O中,溶液颜色介于黄色和橙色之间,今欲使CrO42-的物质的量增大,可以在溶液中加入①H+ ②OH- ③K+ ④CO32-.( )
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
11.一定条件下,可逆反应2A?B+3C,在下列四种状态中处于平衡状态的是( )
正反应速率 逆反应速率.
正反应速率 逆反应速率.
| A. | v(A)=2mol/(L•min) v(B)=2mol/(L•min) | |
| B. | v(A)=2mol/(L•min) v(C)=2mol/(L•min) | |
| C. | v(A)=1mol/(L•min) v(B)=2mol/(L•min) | |
| D. | v(A)=1mol/(L•min) v(C)=1.5mol/(L•min) |
12.我国西部地区蕴藏着丰富的锂资源,开发锂的用途是一个重要的科学课题.关于锂的叙述不正确的是( )
| A. | 锂是较轻的金属 | B. | LiOH的碱性比NaOH弱 | ||
| C. | 锂的化学性质比钠活泼 | D. | 锂在空气中燃烧生成Li2O |
 X、Y、Z、W、U为原子序数依次增大的前四周期元素,X、Y、Z三种元素位于第二周期且相邻,W是非金属元素,其中基态Y原子的2p轨道处于半充满状态,基态W原子的3p能级上有一个未成对电子.含U的化合物的焰色为紫色.试回答下列问题:
X、Y、Z、W、U为原子序数依次增大的前四周期元素,X、Y、Z三种元素位于第二周期且相邻,W是非金属元素,其中基态Y原子的2p轨道处于半充满状态,基态W原子的3p能级上有一个未成对电子.含U的化合物的焰色为紫色.试回答下列问题: .
.