题目内容
11.一定条件下,可逆反应2A?B+3C,在下列四种状态中处于平衡状态的是( )正反应速率 逆反应速率.
| A. | v(A)=2mol/(L•min) v(B)=2mol/(L•min) | |
| B. | v(A)=2mol/(L•min) v(C)=2mol/(L•min) | |
| C. | v(A)=1mol/(L•min) v(B)=2mol/(L•min) | |
| D. | v(A)=1mol/(L•min) v(C)=1.5mol/(L•min) |
分析 化学反应到达平衡时,同一物质的正逆反应速率相等,据此分析判断.
解答 解:化学反应到达平衡时,同一物质的正逆反应速率相等.
A、同一反应中,各物质的反应速率之比等于计量数之比,B物质的逆反应速率是2 mol/(L.min),A的逆反应速率为4mol/(L.min),A的正反应速率为2mol/(L.min),所以A的正逆反应速率不等,故A错误;
B、同一反应中,各物质的反应速率之比等于计量数之比,C物质的逆反应速率是2mol/(L.min),A的逆反应速率为$\frac{4}{3}$mol/(L.min),A的正反应速率为2mol/(L.min),所以A的正逆反应速率不等,故B错误;
C、同一反应中,各物质的反应速率之比等于计量数之比,B物质的逆反应速率是2 mol/(L.min),A的逆反应速率为4mol/(L.min),A的正反应速率为1mol/(L.min),所以A的正逆反应速率不等,故C错误;
D、同一反应中,各物质的反应速率之比等于计量数之比,C物质的逆反应速率是1.5 mol/(L.min),A的逆反应速率为1mol/(L.min),A的正反应速率为1mol/(L.min),所以A的正逆反应速率相等,故D正确;
故选D.
点评 本题考查了化学平衡状态的判断,难度不大,注意:正逆反应速率相等是指同一物质的正逆反应速率相等.

练习册系列答案
相关题目
2.除去下列杂质(括号内是杂质)所用试剂不正确的是( )
| A. | CO2(HCl):用饱和NaHCO3溶液 | B. | CO2(SO2):用饱和KMnO4溶液 | ||
| C. | Cl2(HCl):用饱和NaCl溶液 | D. | SO2(HCl):用饱和NaOH溶液 |
19.化学与社会、科学、技术、环境等有密切关系.下列说法不正确的是( )
| A. | 司母戊鼎、定远舰甲板、有机玻璃等原材料属于合金 | |
| B. | 氯气是塑料、合成橡胶、合成纤维、农药、染料及药品的重要原料 | |
| C. | 工业上生产玻璃、水泥、漂白粉均需要用石灰石为原料 | |
| D. | 用浸泡过溴的四氯化碳溶液的硅藻土吸收水果产生的乙烯以达到保鲜目的 |
16.近年来,我国多地频现种种极端天气,二氧化碳、氮氧化物、二氧化硫是导致极端天气的重要因素.
(1)活性炭可用于处理大气污染物NO,在1L恒容密闭容器中加入0.100mol NO和2.030mol固体活性炭(无杂质),生成气体E和气体F.当温度分别在T1℃和T2℃时,测得平衡时各物质的物质的量如下表:
①结合上表数据,写出NO与活性炭反应的化学方程式C+2NO?N2+CO2;
②上述反应的平衡常数表达式K=$\frac{c({N}_{2})c(C{O}_{2})}{{c}^{2}(NO)}$,根据上述信息判断,T1和T2的关系是C;
A.T1>T2B.T1<T2C.无法比较
③在T1℃下反应达到平衡后,下列措施能改变NO的转化率的是cd;
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得H2,具体流程如图1所示
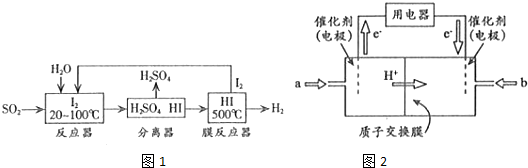
①用离子方程式表示反应器中发生的反应SO2+I2+2H2O=SO42-+2I-+4H+;
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行;
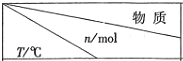
(3)开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图2所示
通过a气体的电极是原电池的负极(填“正”或“负”),b电极反应式为O2+4e-+4H+=2H2O.
(1)活性炭可用于处理大气污染物NO,在1L恒容密闭容器中加入0.100mol NO和2.030mol固体活性炭(无杂质),生成气体E和气体F.当温度分别在T1℃和T2℃时,测得平衡时各物质的物质的量如下表:
 | 活性炭 | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②上述反应的平衡常数表达式K=$\frac{c({N}_{2})c(C{O}_{2})}{{c}^{2}(NO)}$,根据上述信息判断,T1和T2的关系是C;
A.T1>T2B.T1<T2C.无法比较
③在T1℃下反应达到平衡后,下列措施能改变NO的转化率的是cd;
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得H2,具体流程如图1所示

①用离子方程式表示反应器中发生的反应SO2+I2+2H2O=SO42-+2I-+4H+;
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行;
(3)开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图2所示
通过a气体的电极是原电池的负极(填“正”或“负”),b电极反应式为O2+4e-+4H+=2H2O.
20.在NaCl、MgCl2、MgSO4形成的混合溶液中,c(Na+)=0.20mol/L,c(Mg2+)=0.50mol/L,c(Cl-)=0.20mol/L,则c(SO42-)为( )
| A. | 0.15mol/L | B. | 0.10mol/L | C. | 0.50mol/L | D. | 0.20mol/L |
1.已知T、X、Y、Z是中学化学常见的四种元素,其结构或性质信息如表:
请根据信息回答有关问题:
(1)写出与Y2互为等电子体的分子式CO;
(2)T、X、Y三种元素的电负性由大到小的顺序(填元素符号)是N>C>Na;
(3)元素Q的原子序数是X与Z的原子序数之和.
①该元素基态原子的外围电子排布式为3d84s2;
②元素Q与元素T、Y、Z分别形成平面型的[Q(TY)4]2-和四面体的[QZ4]2-,Q的配位数为4,其中T与Y、Q与Z成键时中心原子采用的杂化方式分别是sp、sp3.
| 元素 | 结构或性质信息 |
| T | 原子的L层上s电子数等于p电子数. |
| X | 元素的原子半径是第三周期主族元素中最大的. |
| Y | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的. |
| Z | 单质常温、常压下是气体.原子的M层上有1个未成对的p电子. |
(1)写出与Y2互为等电子体的分子式CO;
(2)T、X、Y三种元素的电负性由大到小的顺序(填元素符号)是N>C>Na;
(3)元素Q的原子序数是X与Z的原子序数之和.
①该元素基态原子的外围电子排布式为3d84s2;
②元素Q与元素T、Y、Z分别形成平面型的[Q(TY)4]2-和四面体的[QZ4]2-,Q的配位数为4,其中T与Y、Q与Z成键时中心原子采用的杂化方式分别是sp、sp3.