题目内容
16.25℃四种水溶液①HCl,②FeCl3,③KOH,④Na2CO3其 pH值依次为4、4、10、10,而溶液中水的电离程度大小关系正确的是( )| A. | ①=②=③=④ | B. | ①=③>②=④ | C. | ④=②>③=① | D. | ①>③>②>④ |
分析 酸或碱抑制水电离,酸中氢离子或碱中氢氧根离子浓度越大其抑制水电离程度越大;含有弱离子的盐促进水电离,弱离子水解程度越大则水的电离程度越大,据此分析解答.
解答 解:酸或碱抑制水电离,酸中氢离子或碱中氢氧根离子浓度越大其抑制水电离程度越大;含有弱离子的盐促进水电离,弱离子水解程度越大则水的电离程度越大,
①是酸、③是碱,所以二者抑制水电离,且酸中氢离子浓度等于碱中氢氧根离子浓度,所以二者抑制水电离程度相同;
②、④都是含有弱离子的盐,根据溶液的pH知,二者水解程度相同,所以促进水电离程度相同,
则水的电离程度大小顺序是④=②>③=①,
故选C.
点评 本题考查盐类水解、水电离影响因素,为高频考点,明确哪些物质促进水电离、哪些物质抑制水电离是解本题关键,酸或碱抑制水电离程度与溶液中氢离子或氢氧根离子浓度有关,与电解质强弱无关.

练习册系列答案
相关题目
6.下列有关有机反应类型的判断错误的是( )
| A. | CH2═CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH 加成反应 | |
| B. | 2CH3CH2OH $?_{140℃}^{浓硫酸}$CH3CH2OCH2CH3+H2O 消去反应 | |
| C. | 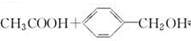 $?_{△}^{浓硫酸}$ $?_{△}^{浓硫酸}$ 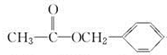 +H2O取代反应 +H2O取代反应 | |
| D. | 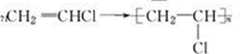 加聚反应 加聚反应 |
7.25℃时,水的电离达到平衡:H2O?H++OH-△H>0,下列叙述正确的是( )
| A. | 向水中加入稀氨水,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 | |
| C. | 向水中加入少量固体NaOH,平衡逆向移动,c(H+)降低,KW减小 | |
| D. | 将水加热,KW增大,pH不变 |
4.在强酸性溶液中能大量共存,并且溶液透明的是( )
| A. | K+、Ca2+、HCO3-、Cl- | B. | Cu2+、Na+、NO3-、Cl- | ||
| C. | Na+、Fe3+、SO42-、CO32- | D. | Mg2+、NH4+、Cl-、OH- |
11.以NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol Cu与含2 mol H2SO4的浓硫酸加热反应,转移的电子数为 2 NA | |
| B. | 5.80g[2 CaSO4.H2O]中含有的H2O分子数为0.04NA(M(2 CaSO4.H2O)=290g.nol-1) | |
| C. | 0.1 mol BaO2与足量的CO2完全反应转移电子数目为0.1NA | |
| D. | 10 mL 5 mol•L-1(NH4)2CO3溶液中含有N原子数目小于0.1 NA |
8.下列各组物质能相互反应,最终能生成氢氧化铝的是( )
| A. | 铝和氢氧化钠溶液共热 | |
| B. | 氯化铝溶液中滴入过量氢氧化钾溶液 | |
| C. | 明矾溶液中滴入过量氨水 | |
| D. | 物质的量浓度相同的硝酸铝溶液和氢氧化钠溶液等体积混合 |