题目内容
7.25℃时,水的电离达到平衡:H2O?H++OH-△H>0,下列叙述正确的是( )| A. | 向水中加入稀氨水,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 | |
| C. | 向水中加入少量固体NaOH,平衡逆向移动,c(H+)降低,KW减小 | |
| D. | 将水加热,KW增大,pH不变 |
分析 根据水的电离方程式H2O?H++OH-△H>0知,该反应是吸热反应,且酸或碱抑制水电离,升高温度促进水电离,水的离子积常数只与温度有关,与溶液酸碱性无关,据此分析解答.
解答 解:A.向水中加入稀氨水,一水合氨电离出的OH-导致溶液中c(OH-)增大而抑制水电离,平衡逆向移动,故A错误;
B.加入固体硫酸氢钠,硫酸氢钠电离出H+而使溶液中c(H+)增大,所以抑制水电离,但温度不变,离子积常数不变,故B正确;
C.加入NaOH固体,电离出的OH-导致溶液中c(OH-)增大而抑制水电离,平衡逆向移动,c(H+)降低,但温度不变离子积常数不变,故C错误;
D.升高温度,平衡正向移动,溶液中c(H+)、c(OH-)增大导致离子积常数增大,溶液的pH减小,故D错误;
故选B.
点评 本题考查水的电离及离子积常数,为高频考点,明确离子积常数、水的电离影响因素是解本题关键,注意:离子积常数只与温度有关,与溶液浓度及酸碱性无关,题目难度不大.

练习册系列答案
相关题目
17.下列有关说法中不正确的是( )
| A. | 铁与Cl2、盐酸均能发生反应,但生成的含铁物质组成不同 | |
| B. | 分别加热蒸干并灼烧铁、铝的氯化物溶液,最后得到的物质均为金属氧化物 | |
| C. | 等物质的量的Na、Cu、Al与足量氯气反应时,消耗的氯气一样多 | |
| D. | 常温下,铁片、铝片与浓硫酸的反应均只能停留在金属的表面上 |
18.某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O). 下列说法正确的是( )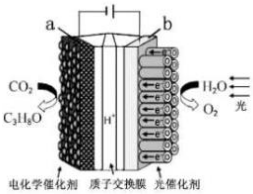

| A. | 该装置将化学能转化为光能和电能 | |
| B. | 该装置工作时,H+从a 极区向b 极区迁移 | |
| C. | 每有44 g CO2被还原,则生成标准状况下 33.6 L O2 | |
| D. | a 电极的反应为:3CO2+16H+-18e-═C3H8O+4H2O |
15.下列叙述错误的是( )
| A. | 用金属钠可区分乙醇和乙醚 | |
| B. | 用高锰酸钾酸性溶液可区分乙烷和乙烯 | |
| C. | 用水可区分苯和溴苯 | |
| D. | 用高锰酸钾酸性溶液可直接除去乙烷中的乙烯 |
2.在下列给定的溶液中一定能大量共存的离子组是( )
| A. | $\frac{{K}_{W}}{C({H}^{+})}$=0.1mol/L的溶液中:K+、Fe2+、Cl?、NO-3 | |
| B. | 水电离的H+浓度为1×10-12 mol/L的溶液:K+、Ba2+、Cl-、Br- | |
| C. | 加入NH4HCO3固体产生气泡的溶液中:Na+、Mg2+、ClO-、S2- | |
| D. | 加金属铝能产生氢气的溶液中:Ca2+、NH4+、Cl-、HSO3- |
12.下列关于SO2的说法中,不正确的是( )
| A. | SO2可使石蕊试液褪色 | B. | SO2有漂白和杀菌作用 | ||
| C. | SO2溶于水后生成H2SO4 | D. | SO2是一种大气污染物 |
19.下列反应的离子方程式书写正确的是( )
| A. | 氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
16.25℃四种水溶液①HCl,②FeCl3,③KOH,④Na2CO3其 pH值依次为4、4、10、10,而溶液中水的电离程度大小关系正确的是( )
| A. | ①=②=③=④ | B. | ①=③>②=④ | C. | ④=②>③=① | D. | ①>③>②>④ |
17.下列物质属于共价化合物的是( )
| A. | MgO | B. | CO2 | C. | NH4Cl | D. | N2 |