题目内容
16.如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )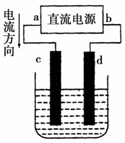
| A. | a为负极、b为正极 | B. | c为阴极、d为阳极 | ||
| C. | 电解过程中,d电极质量不变 | D. | 电解过程中,氯离子浓度减小 |
分析 由电流从正极流向负极可知,a为正极,c为阳极,阳极上氯离子失去电子生成氯气,d为阴极,阴极上铜离子得到电子生成Cu,以此来解答.
解答 解:A.由电流方向可知,a为正极,b为负极,故A错误;
B.c与a相连,a为阳极,故B错误;
C.d为阴极,阴极上铜离子得到电子生成Cu,则d电极质量增加,故C错误;
D.发生CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑,电解过程中,氯离子浓度减小,故D正确;
故选D.
点评 本题考查电解原理及应用,为高频考点,把握电极、电极反应、电流方向为解答的关键,侧重分析与应用能力的考查,注意利用电流方向判断电极,题目难度不大.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案
相关题目
3.下列离子方程式书写正确的是( )
| A. | 铁粉放入稀硫酸溶液:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 往NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 石灰石与稀盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | Cl2通入水中:Cl2+H2O?H++Cl-+HClO |
4.某溶液中只可能含有下列离子中的几种:Na+、NH4+、SO42-、CO32-、NO3-、Cl-(不考虑溶液中少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
(1)第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;
(2)第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g.
(3)在(2)的滤液中滴入AgNO3,产生白色沉淀,加稀硝酸,沉淀不溶解.
下列说法正确的是( )
(1)第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;
(2)第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g.
(3)在(2)的滤液中滴入AgNO3,产生白色沉淀,加稀硝酸,沉淀不溶解.
下列说法正确的是( )
| A. | 该溶液中可能含Na+ | B. | 该溶液中肯定含有NH4+、SO42-、Cl- | ||
| C. | 该溶液中一定不含NO3-、CO3- | D. | 该溶液中一定含有Na+ |
8.在含有大量Fe3+、H+、SO42-的溶液中,还可能大量共存的离子是( )
| A. | Ba2+ | B. | OH- | C. | I- | D. | NH4+ |
5.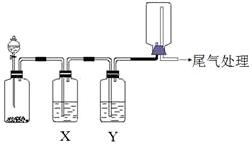 利用图装置可以进行实验并能达到实验目的是( )
利用图装置可以进行实验并能达到实验目的是( )
 利用图装置可以进行实验并能达到实验目的是( )
利用图装置可以进行实验并能达到实验目的是( )| 选项 | 实验目的 | X中试剂 | Y中试剂 |
| A | 用MnO2和浓盐酸制取并收集纯净干燥的Cl2 | 饱和食盐水 | 浓硫酸 |
| B | 用Cu与稀硝酸制取并收集纯净干燥的NO | 水 | 浓硫酸 |
| C | 用CaO于浓氨水制取并收集纯净干燥的NH3 | NaOH溶液 | 碱石灰 |
| D | CaCO3和稀盐酸制取并收集纯净干燥的CO2 | 饱和NaHCO3溶液 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
6.化学中常用图象直观地描述化学反应的进程或结果.下列图象描述正确的是( )
| A. |  图表示不同压强对反应体系3X(g)?2Y(g)+Z(s)中X体积分数的影响 | |
| B. |  图表示CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化 | |
| C. |  图中的线条2表示放热反应2H2O2═2H2O+O2加入催化剂Br2的反应进程 | |
| D. |  图表示用0.1000mol•L-1NaOH溶液分别滴定同浓度同体积盐酸和醋酸的曲线 |
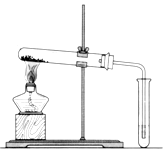 碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)都可作为食用碱.
碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)都可作为食用碱.