题目内容
1.25°C时,如图烧杯中各盛有50mL的溶液.
(1)甲溶液PH=2;
(2)若将甲溶液全部倒入乙中,所得的混合溶液的PH>丙溶液的PH(填“>”、“<”或“=”).
(3)若将乙溶液全部倒入丙中,所得的混合溶液PH>7,所得溶液中离子浓度大小顺序是c(NH4+)>c(Cl-)>c(OH-)>c(H+).
分析 (1)根据pH=-lgc(H+)计算0.01mol/L盐酸的pH;
(2)等体积等物质的量浓度的盐酸和氨水恰好反应生成氯化铵,氯化铵是强酸弱碱盐,其溶液呈酸性,浓度不同的氯化铵溶液,浓度越小,其溶液的PH越大;
(3)若将乙溶液全部倒入丙中,所得的混合溶液pH>7,说明一水合氨是电离程度大于铵根离子的水解程度,根据溶液的酸碱性结合电荷守恒确定离子浓度大小.
解答 解:(1)氯化氢是强电解质,在水中完全电离,所以c(H+)=c(HCl)=0.01mol/L,所以pH=-lgc(H+)=-lg0.01=2,
故答案为:2;
(2)等体积等物质的量浓度的盐酸和氨水恰好反应生成氯化铵,氯化铵是强酸弱碱盐,其溶液呈酸性,溶液混合时体积增大一倍,浓度是丙中的一半,氯化铵的浓度越小,其酸性越弱,所以混合溶液的pH大于丙,
故答案为:>;
(3)若将乙溶液全部倒入丙中,所得的混合溶液pH>7,说明一水合氨是电离程度大于铵根离子的水解程度,所以得c(OH-)>c(H+),根据电荷守恒c(NH4+)+c(H+)=c(Cl-)+c(OH-)可知:c(NH4+)>c(Cl-),则溶液中离子浓度大小顺序是:c(NH4+)>c(Cl-)>c(OH-)>c(H+),
故答案为:c(NH4+)>c(Cl-)>c(OH-)>c(H+).
点评 本题考查了溶液酸碱性与溶液pH的计算,题目难度中等,明确溶液酸碱性与溶液pH的关系即可解答关键,注意掌握判断离子浓度大小的常用方法,试题培养了学生的灵活应用能力.

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
12.分子式为C8H8的有机物X,X核磁共振氢谱显示只有一个吸收峰,下列相关说法正确的是( )
| A. | X是乙烯 | B. | X能使溴水褪色 | ||
| C. | X属于不饱和烃 | D. | X的二氯代物有三种 |
9.下列离子方程式的书写正确的是( )
| A. | 大理石溶于醋酸中:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| B. | H2SO4溶液与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 将Na投入到CuSO4溶液中:2Na+Cu2+═2Na++Cu↓ | |
| D. | 将Cl2通入水中:Cl2+H2O═2H-+Cl-+ClO- |
16.如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )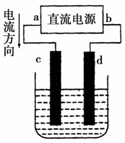

| A. | a为负极、b为正极 | B. | c为阴极、d为阳极 | ||
| C. | 电解过程中,d电极质量不变 | D. | 电解过程中,氯离子浓度减小 |
6.下列物质中既含有离子键又含有共价键的是( )
| A. | NH4Cl | B. | NaCl | C. | H2O | D. | Cl2 |
13.用下列图示操作,装置正确且能达到实验目的是( )
| A. |  制取氨气 | B. |  干燥氯气 | C. |  转移溶液 | D. |  萃取溴 |
10.下列与化学有关的说法中正确的是( )
| A. | 在0.1mol/lHNO3溶液中加入FeCO3粉末,发生反应的离子方程式为:2FeCO3+2H+═2Fe2++CO2↑+H2O | |
| B. | 在$\frac{c(O{H}^{-})}{c({H}^{+})}$=1010的溶液中NO3-、I-、Na+、SO42-不能大量共存 | |
| C. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1 NA | |
| D. | 闭容器中2molNO与1molO2充分反应,产物的分子数小于2NA |
11.常温下,下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 将浓度均为0.10mol•L-1的CH3COONH4与CH3COONa溶液等体积混合:c(CH3COO-)>c(Na+)>c(NH4+)>c(OH-) | |
| B. | 向0.10mol•L-1CH3COONa溶液中滴加盐酸至溶液呈中性:c(Cl-)>c(Na+)>c(H+)=c(OH-) | |
| C. | 将0.10mol•L-1KHC2O4和0.10mol•L-1K2C2O4溶液等体积混合所得溶液中:2c(K+)=3c(C2O42-)+3c(HCO4) | |
| D. | 将等物质的量浓度的NH4HCO3与NaCl溶液等体积混合,析出部分NaHCO3晶体后的溶液(pH<7)中:c(H+)+c(H2CO3)=c(OH-)+c(CO32-)+c(NH3•H2O) |