题目内容
铝在人体中积累可使人慢性中毒,世界卫生组织将铝确定为食品污染源之一,应该严加控制.铝在下列使用场合中,必须加以控制的是( )
| A、制造电缆 |
| B、制防锈油漆 |
| C、制饮料罐 |
| D、炼铝厂制造铝锭 |
考点:微量元素对人体健康的重要作用
专题:
分析:铝在人体内积累可使人慢性中毒,铝进入人体的主要途径是通过消化系统,既然铝是食品污染源之一,凡与人的食用物品及口腔接触的物品都必须控制铝的使用.
解答:
解:A、铝作电线电缆与人的消化系统不直接接触,铝不会因使用电缆进入人体,故A错误;
B、用铝制防锈油漆,正常情况下铝与人的消化系统不直接接触,铝不会因使用电缆进入人体,与人体健康无关,无需控制,故B错误;
C、用铝制作饮料罐时,会使铝进入人体,需要加以控制,故C正确;
D、炼铝厂制造铝锭,铝不与人的消化系统不直接接触,铝不会因此进入人体,故D错误.
故选C.
B、用铝制防锈油漆,正常情况下铝与人的消化系统不直接接触,铝不会因使用电缆进入人体,与人体健康无关,无需控制,故B错误;
C、用铝制作饮料罐时,会使铝进入人体,需要加以控制,故C正确;
D、炼铝厂制造铝锭,铝不与人的消化系统不直接接触,铝不会因此进入人体,故D错误.
故选C.
点评:“关爱生命,拥抱健康”是人类追求的永恒主题,对营养元素与人体健康的考查也就成了热点之一,特别是元素的分类、元素的生理功能和对人体的影响等内容.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
把0.02mol?L-1 CH3COOH溶液和0.01mol?L-1 NaOH溶液以等体积混合,混合溶液中粒子浓度关系正确的是( )
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COOH)>c(CH3COO-) |
| C、c(H+)<c(OH-) |
| D、c(CH3COO-)>+c(CH3COOH)=0.02mol?L-1 |
已知反应4A(g)?2B(g)+E(g)△H>0.达到平衡时,要使正反应速率降低,A的浓度增大,可以采取的措施是( )
| A、增大压强 | B、减小压强 |
| C、减少E的浓度 | D、降温 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为下列叙述不正确的是( )3Zn+2K2FeO4+5H2O
3zs(OH)2+2Fe(OH)3+4KOH.
| 放电 |
| 充电 |
| A、放电时负极反应为:Zn+2OH--2e-═Zn(OH)2 |
| B、充电时阳极反应为:Fe(OH)3+5OH--3e-═FeO42-+4H2O |
| C、放电时每转移3mol电子,正极有1mol K2FeO4被氧化 |
| D、放电时正极附近溶液的碱性增强 |
1mol气态钠离子和1mol气态氯离子结合生成1mol氯化钠晶体释放出的热能为氯化钠晶体的晶格能.下列热化学方程式中,能直接表示出氯化钠晶体晶格能的是( )
| A、Na+(g)+Cl-(g)═NaCl(s)△H |
| B、Na(s)+12Cl2(g)═NaCl(s)△H1 |
| C、Na(g)-e-═Na+(g)△H2 |
| D、Cl(g)+e-═Cl-(g)△H3 |
两种元素X、Y,其原子核外电子层数分别为a、b,最外层电子数分别为m、n.下列说法错误的是( )
| A、若a=b=3,8>m>n>b,则元素非金属性:X>Y |
| B、若a<b<m=n=4,则晶体类型相同时,其单质熔点:Y<X |
| C、若Y的气态氢化物化学式为YHn,且b<4,则该氢化物易溶于水 |
| D、若a<b=3,m=n=7,已知原子半径大小:Y>N(氮原子)>X,则NX3、NY3与水反应生成不同的含氮化合物 |
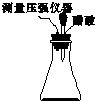 某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图所示).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图所示).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.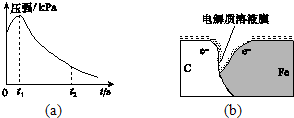 (3)该小组对图(a)中0~t1时压强变大的原因提出了如下假设,请你完成假设二:
(3)该小组对图(a)中0~t1时压强变大的原因提出了如下假设,请你完成假设二: