��Ŀ����
13��һ���Ի�ͭ������Ϊԭ����ȡͭ������������¹��յ���Ҫ�������£�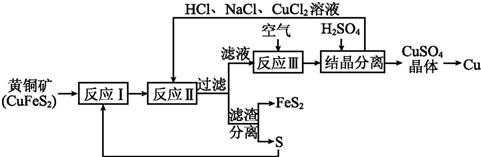
�����������У���Ӧ��Ļ�ѧ������ΪCuFeS2+S�TFeS2+CuS����Ӧ����Һ����Ҫ�ɷ�Ϊ[CuCl2]-����ش��������⣺
��1��Ϊʹ��Ӧ���ֽ��У���ҵ�Ͽɲ�ȡ�Ĵ�ʩ�Ƿ������ȣ����1�㼴�ɣ���
��2����Ӧ������ӷ���ʽΪCu2++CuS+4Cl-=2[CuCl2]-+S����
��3����Ӧ��ͨ�������Ŀ���ǽ���Ӧ�����ɵ�һ��ͭ�����ɶ���ͭ�� һ���¶��£��ڷ�Ӧ�����õ���Һ�м���ϡ���ᣬ������������ͭ���壬��ԭ��������ͭ���ܽ��С���Ȼ�ͭ���ܽ�ȣ�
��4����CuSO4�Ƶ�Cu�ɲ�ȡ��ʪ����ͭ�����÷�Ӧ�����ӷ���ʽ��Fe+Cu2+=Fe2++Cu�������������̵���Ҫ�ص���ԭ�ϵ��ۺ������ʽϸߣ�
��5���Ի�ͭ����Ҫ�ɷ�ΪCuFeS2��Ϊԭ���Ʊ�ͭ��Ҳ���Բ��á����������ա��������������ա��еġ����ա���������ͨ�����������������ʹ��ͭ���������ɱ�ɰ����Ҫ�ɷ���Cu2S��FeO����SO2���÷�Ӧ�Ļ�ѧ����Ϊ2CuFeS2+4O2$\frac{\underline{\;����\;}}{\;}$Cu2S+3SO2+2FeO��
���� �����з�Ӧ��Ļ�ѧ������ΪCuFeS2+S�TFeS2+CuS����ͭ����S�ڸ��������գ�ʹ��ת��ΪFeS2��CuS������HCl��NaCl��CuCl2�����Һ ������ӦCu2++CuS+4Cl-=2[CuCl2]-+S�������˵õ���Һ��ͨ�����������Ӧ4CuCl2-+O2+4H+=4Cu2++8Cl-+2H2O��һ���¶��£��ڷ�Ӧ�����õ���Һ�м���ϡ���ᣬ������������ͭ���壬�ᾧ����õ�����ͭ���壬��������ԭ��Һ�õ�ͭ����������õ�FeS��S��
��1����������������Ӵ�������ӿ췴Ӧ���ʣ�
��2�����ڷ�Ӧ1֮�������ֲ��������������ͭ����������Ӧ���ٹ���֮����������ʣ�࣬˵���ڷ�Ӧ���б����ĵ���������ͭ��
��3�������������ԣ����Խ���Ӧ�����ɵ�һ��ͭ�����ɶ���ͭ��������������������ͭ������Ϊ����ͭ���ܽ��С���Ȼ�ͭ���ܽ�ȣ�
��4����CuSO4�Ƶ�Cu�ɲ�ȡ��ʪ����ͭ�����������������û���Ӧ��������ԭ�������ʸߣ�
��5���ɷ�Ӧ������P�����غ㶨������д����ʽ��
��� �⣺�����з�Ӧ��Ļ�ѧ������ΪCuFeS2+S�TFeS2+CuS����ͭ����S�ڸ��������գ�ʹ��ת��ΪFeS2��CuS������HCl��NaCl��CuCl2�����Һ ������ӦCu2++CuS+4Cl-=2[CuCl2]-+S�������˵õ���Һ��ͨ�����������Ӧ4CuCl2-+O2+4H+=4Cu2++8Cl-+2H2O��һ���¶��£��ڷ�Ӧ�����õ���Һ�м���ϡ���ᣬ������������ͭ���壬�ᾧ����õ�����ͭ���壬��������ԭ��Һ�õ�ͭ����������õ�FeS��S��
��1����������������Ӵ�������ӿ췴Ӧ���ʣ���Ϊʹ��Ӧ���ֽ��У���ҵ�Ͽɲ�ȡ�Ĵ�ʩ�Ƿ������ȣ�
�ʴ�Ϊ���������ȣ�
��2�����ڷ�Ӧ1֮�������ֲ��������������ͭ����������Ӧ���ٹ���֮����������ʣ�࣬˵���ڷ�Ӧ���б����ĵ���������ͭ����Ӧ������ӷ���ʽΪCu2++CuS+4Cl-=2[CuCl2]-+S�����ʴ�Ϊ��Cu2++CuS+4Cl-=2[CuCl2]-+S����
��3�������������ԣ���֪��Ӧ��ͨ�������Ŀ���ǽ���Ӧ�����ɵ�һ��ͭ�����ɶ���ͭ��������������������ͭ������Ϊ����ͭ���ܽ��С���Ȼ�ͭ���ܽ�ȣ�
�ʴ�Ϊ������Ӧ�����ɵ�һ��ͭ�����ɶ���ͭ������ͭ���ܽ��С���Ȼ�ͭ���ܽ�ȣ�
��4����CuSO4�Ƶ�Cu�ɲ�ȡ��ʪ����ͭ�����������������û���Ӧ����ӦΪFe+Cu2+=Fe2++Cu�������������̵���Ҫ�ص���ԭ�ϵ��ۺ������ʽϸߣ�
�ʴ�Ϊ��Fe+Cu2+=Fe2++Cu��ԭ�ϵ��ۺ������ʽϸߣ�
��5���ɷ�Ӧ������P�����غ㶨�ɿ�֪�����ķ�ӦΪ2CuFeS2+4O2$\frac{\underline{\;����\;}}{\;}$Cu2S+3SO2+2FeO���ʴ�Ϊ��2CuFeS2+4O2$\frac{\underline{\;����\;}}{\;}$Cu2S+3SO2+2FeO��
���� ���⿼���Ʊ�ʵ�鷽������ƣ�Ϊ��Ƶ���㣬�����Ʊ�ʵ�����̡����������ᴿ�������ķ�ӦΪ���Ĺؼ������ط�����ʵ���������ۺϿ��飬ע����ϰ���е���Ϣ����������Ŀ�Ѷ��еȣ�

 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д�| A�� | ��Һ�е������ӵ���Ŀ���ӣ���������ǿ | |
| B�� | ��ˮ�ĵ���̶�����[OH-]��С | |
| C�� | �ټ���10mL pH=3 HCl��Һ�����ҺpH=7 | |
| D�� | ��Һ����ˮ�������[OH-]=1��10-3 mol•L-1 |
| ������ | ��Է������� | �ܶ�/g•cm-3 | �е㣬/�� | �ܽ��/l00gˮ |
| ������ | 74 | 0.80 | 118.0 | 9 |
| ������ | 60 | 1.045 | 118.1 | ���� |
| ���������� | 116 | 0.882 | 126.1 | 0.7 |
����50mL������ƿ�У�����18.5mL��������13.4mL�����ᣬ3��4��Ũ���ᣬͶ���ʯ����װ��ˮ�������ã�ʵ������в��Ϸ����ȥ��Ӧ���ɵ�ˮ�����¶ȼƼ����������ܣ�
�ڽ���ˮ���ֳ�������ͷ�ӦҺһ�����Һ©���У�ˮϴ��10% Na2CO3ϴ�ӣ���ˮϴ�����ת������ƿ�����
�۽�����������������������ƿ�У���ѹ�����ռ���֣���15.1g������������
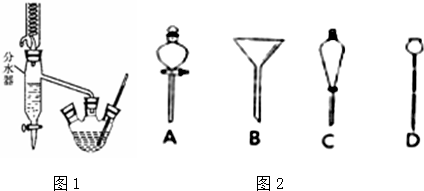
��ش��й����⣺
��1����ˮӦ�ô�������a����a��b���˹ܿ�ͨ�룮
��2������A�з�����Ӧ�Ļ�ѧ����ʽΪCH3COOH+CH3CH2CH2CH2OH
 CH3COOCH2CH2CH2CH3+H2O��
CH3COOCH2CH2CH2CH3+H2O����3������١����Ϸ����ȥ��Ӧ���ɵ�ˮ���ò�����Ŀ���ǣ�ʹ�÷�ˮ�������ˮ��ʹƽ�������ƶ�����߷�Ӧ���ʣ�
��4�����������10%Na2CO3��Һϴ���л��㣬�ò�������Ŀ���dz�ȥ��Ʒ�к��е���������ʣ�
��5�����з�Һ����ʱ��ʹ�õ�©����C����ѡ���
��6��������ڽ����������ʱ������118�濪ʼ�ռ���֣�����ƫ�ߣ���ߡ����ߡ��͡���ԭ���ǻ��ռ�������δ��Ӧ�ı������������
��7����ʵ������У����������������IJ�����65%��
| A�� | ��NaClO��Һ��ͨ�����SO2��ClO-+SO2+H2O�THClO+HSO3- | |
| B�� | Na2SͶ��ˮ�У�S2-+2H2O?H2S+2OH- | |
| C�� | ��1molAlCl3��Һ��Ͷ��4molNa��Al3++4Na+2H2O�TAlO2-+4Na++2H2�� | |
| D�� | ��������Һ�еμ�Ba��OH��2��Һ��ǡ��ʹSO42-������ȫ��2Al3++3SO42-+3Ba2++6OH-�TAl��OH��3��+3BaSO4�� |
| A�� | NaCl���塢BaSO4 | B�� | ������������ | ||
| C�� | Һ̬�Ĵ��ᡢ�ƾ� | D�� | ���ڵ�KNO3��������Һ |
| A�� | 0.8mol/��L•s�� | B�� | 2.0mol/��L•s�� | C�� | 4.0mol/��L•s�� | D�� | 6.0mol/��L•s�� |
 ̫���ܵ����ͨ�����ЧӦ���߹⻯ѧЧӦֱ�Ӱѹ���ת���ɵ��ܵ�װ�ã�����ϳ������裬����ͭ�������Ȼ����
̫���ܵ����ͨ�����ЧӦ���߹⻯ѧЧӦֱ�Ӱѹ���ת���ɵ��ܵ�װ�ã�����ϳ������裬����ͭ�������Ȼ����