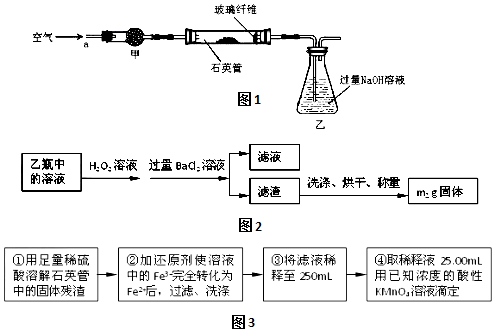
题目内容
6.紫水晶在西方国家代表着“爱的守护石”,其主要成分SiO2属于( )| A. | 碱性氧化物 | B. | 酸性氧化物 | C. | 碱 | D. | 盐 |
分析 根据氧化物的组成和性质特点进行分析,由两种元素组成,其中一种是氧元素的化合物是氧化物.
解答 解:SiO2是由两种元素组成,其中一种是氧元素的化合物,是氧化物,且二氧化硅与碱反应生成盐与水,所以二氧化硅是酸性氧化物,故选B.
点评 本题考查了氧化物的概念和辨析,根据定义可知,氧化物只能含有两种元素,而且其中一种必须是氧元素.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下列解释事实的离子方程式正确的是( )
| A. | SO2通入Ba(NO3)2溶液中有白色沉淀:SO2+Ba2++H2O═BaSO3↓+2H+ | |
| B. | 0.1mol/L氨水的pH为11:NH3•H2O?NH4++OH- | |
| C. | “84”消毒液和“洁厕灵”(主要成分为盐酸)混合使用会产生有毒气体:ClO3-+Cl-+6H+═Cl2+3H2O | |
| D. | 氯化铁溶液中滴加氢硫酸溶液:2Fe3++S2-═2Fe2++S↓ |
11.下列气体不能用排空气法收集的是( )
| A. | NH3 | B. | SO2 | C. | NO | D. | H2 |
18.新型Na-CO2电池工作原理为:4Na+3CO2═2Na2CO3+C,下列说法正确的是( )
| A. | Na是氧化剂 | B. | CO2在反应中失去电子 | ||
| C. | CO2全部被还原 | D. | 每生成1 molNa2CO3转移2 mol电子 |
16. X、Y、Z、W处于同一周期的四种短周期元素,其原子序数逐渐增大,X、W分别是本周期原子半径最大和最小的主族元素,Y单质在工业上用电解其氧化物的方法制取,Y、Z形成的单质有如下转化关系图.下列说法正确的是( )
X、Y、Z、W处于同一周期的四种短周期元素,其原子序数逐渐增大,X、W分别是本周期原子半径最大和最小的主族元素,Y单质在工业上用电解其氧化物的方法制取,Y、Z形成的单质有如下转化关系图.下列说法正确的是( )
 X、Y、Z、W处于同一周期的四种短周期元素,其原子序数逐渐增大,X、W分别是本周期原子半径最大和最小的主族元素,Y单质在工业上用电解其氧化物的方法制取,Y、Z形成的单质有如下转化关系图.下列说法正确的是( )
X、Y、Z、W处于同一周期的四种短周期元素,其原子序数逐渐增大,X、W分别是本周期原子半径最大和最小的主族元素,Y单质在工业上用电解其氧化物的方法制取,Y、Z形成的单质有如下转化关系图.下列说法正确的是( )| A. | Y、Z形成的化合物可利用离子反应制备 | |
| B. | X、Z形成的化合物可能含共价键 | |
| C. | 化合物XW能促进水的电离 | |
| D. | Y元素只能存在于阳离子中 |
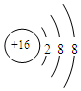 .
.