题目内容
12.下列说法正确的是( )| A. | 按系统命名法,化合物 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| B. | 等物质的量的苯与苯甲酸完全燃烧消耗氧气的量不相等 | |
| C. | 苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 | |
| D. | 等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗用氧气的量依次减少 |
分析 A.根据烷烃命名原则:①长--选最长碳链为主链;②多--遇等长碳链时,支链最多为主链;③近--离支链最近一端编号;④小--支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简--两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面.
B.烃CxHy完全燃烧耗氧量由(x+$\frac{y}{4}$)值决定,(x+$\frac{y}{4}$)的值越大,消耗氧气的量就越多;烃的含氧衍生物CxHyOz完全燃烧耗氧量由(x+$\frac{y}{4}$-$\frac{z}{2}$)值决定,x+$\frac{y}{4}$-$\frac{z}{2}$值越大,消耗氧气的量就越多,据此判断;
C.苯和甲苯互为同系物,但苯不能使KMnO4酸性溶液褪色;
D.等质量的烃,含氢量越高耗氧量越高.
解答 解:A.按系统命名法,化合物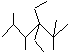
B.苯的x+$\frac{y}{4}$=6+$\frac{6}{4}$=7.5,即1mol苯消耗氧气7.5mol,苯甲酸的x+$\frac{y}{4}$-$\frac{z}{2}$=7+$\frac{6}{4}$-1=7.5,即1mol苯甲酸消耗氧气7.5mol,所以等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等,故B错误;
C.苯和甲苯互为同系物,但苯不能使KMnO4酸性溶液褪色,故C错误;
D.等质量的烃中含氢量越高耗氧量越高,甲烷、乙烯、1,3-丁二烯含H量逐渐降低,则所耗用氧气的量依次减少,故D正确;
故选D.
点评 本题主要考查了物质的命名、燃烧规律、物质的性质,明确键线式、烃及烃的衍生物燃烧规律是解题的关键,题目难度中等.

 精英口算卡系列答案
精英口算卡系列答案| A. | 粮食酿酒 | B. | 食物变质 | C. | 冰雪消融 | D. | 石油裂解 |
(1)基态P原子中,电子占据的最高能级符号为3p,基态N原子核外有7种运动状态不同的电子,基态Br原子的价电子排布式为4S24P5.
(2)HCN的结构式为H-C≡N;其中心C原子的杂化类型为sp杂化.氮、磷、氟三种元素的电负性由大到小的顺序为F>N>P(用元素符号表示).
(3)已知PCl3是不稳定的无色液体,遇水反应可生成两种酸,该反应的化学方程式 为PCl3+3 H2O=H3PO3+3HCl,所得含氧酸(已知该含氧酸的各步电离平衡常数分别为Ka1=1.6×10-2和Ka2=7×10-7)和足量的NaOH溶液反应生成盐的化学式为Na2HPO3.
(4)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是碘(填元素名称)
| F | Cl | Br | I | |
| 第一电离能((kJ•mol-1)) | 1681 | 1251 | 1140 | 1008 |
| A. | CH3CH2OH+CH3COOH $→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O | |
| B. | CH2=CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl | |
| C. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| D. |  |
| A. | 质子数为222 | |
| B. | 中子数为86 | |
| C. | 质量数为308 | |
| D. | 与${\;}_{86}^{219}$Rn、${\;}_{86}^{220}$Rn互为同位素 |
| A. | 电解水生成H2、O2与H2在O2中燃烧生成H2O | |
| B. | H2和I2在高温下边化合边分解 | |
| C. | 溶解与结晶 | |
| D. | SO2通入品红溶液褪色,加热后又恢复红色 |

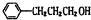 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O;该反应的反应类型为酯化反应或取代反应
+H2O;该反应的反应类型为酯化反应或取代反应 .
.
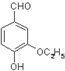 是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称醛基、羟基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称醛基、羟基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.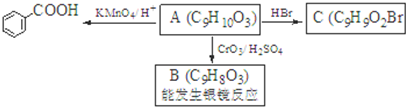
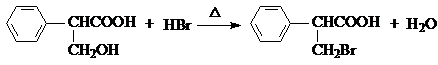 ,属于取代反应(填反应类型).
,属于取代反应(填反应类型). .
. .
. )是一种医药中间体,请设计合理方案用茴香醛(
)是一种医药中间体,请设计合理方案用茴香醛(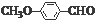 )合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
)合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).

 .
.