题目内容
5.下列关于Na20与Na2O2的说法中,不正确的是( )| A. | Na2O2比Na20化学性质稳定 | |
| B. | 均与水反应生成NaOH,因而均是碱性氧化物 | |
| C. | Na20能被氧化成Na2O2 | |
| D. | 均可与H2O、CO2反应 |
分析 氧化钠可与氧气反应生成过氧化钠,氧化钠可与水反应生成氢氧化钠,为白色固体,与二氧化碳反应生成碳酸钠,而Na2O2为淡黄色固体,可与水、二氧化碳反应生成氧气,Na2O2具有强氧化性,可与具有还原性的物质发生氧化还原反应,以此解答该题.
解答 解:A.因2Na2O+O2═Na2O2,则Na2O2比Na2O稳定,故A正确;
B.过氧化钠与酸反应生成盐、水和氧气,则过氧化钠不属于碱性氧化物,故B错误;
C.2Na2O+O2═Na2O2,Na2O能反应生成Na2O2,故C正确;
D.氧化钠与CO2反应生成碳酸钠,与水反应生成氢氧化钠,过氧化钠与CO2反应生成碳酸钠和氧气,与水反应生成氢氧化钠和氧气,则均与CO2、水反应,故D正确.
故选B.
点评 本题考查钠的重要化合物知识,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握过氧化钠与水、二氧化碳以及酸反应的特点,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M,关于该反应的说法中正确的组合是( )
①氧化剂是H3AsO3; ②还原性:Cl->As; ③每生成0.1mol As,还原剂失去的电子为0.3mol;
④M为OH-; ⑤a=2,b=6.
①氧化剂是H3AsO3; ②还原性:Cl->As; ③每生成0.1mol As,还原剂失去的电子为0.3mol;
④M为OH-; ⑤a=2,b=6.
| A. | 只有①③ | B. | ①③⑤ | C. | ①②③④ | D. | ①②④⑤ |
16.下列有关氯水的说法中,不正确的是( )
| A. | 在通常状况下,新制的氯水呈黄绿色 | |
| B. | 将足量氯水加入到紫色石蕊试液中,溶液只能变成红色 | |
| C. | 将氯水加入到NaHCO3粉末中,有气泡产生 | |
| D. | 将氯水加入到硝酸酸化的AgNO3溶液中,有白色沉淀产生 |
20.下列物质的俗名、化学式或成分、主要用途都正确的是( )
| A. | 福尔马林(纯HCHO):用于浸制生物标本 | |
| B. | 碱石灰(NaOH与CaO的混合物):作碱性干燥剂 | |
| C. | 甲烷(CH4):与氯气反应可制得纯净的一氯甲烷 | |
| D. | 明矾(KAl(SO4)2•12H2O):水解生成Al(OH)3胶体,可用于水的净化 |
10.常态时,下列物质是黄色的是( )
| A. | 铜单质 | B. | 铁锈 | C. | Na2O | D. | Na2O2 |
17.下列实验不能产生气体的是( )
| A. | Na2O投入水中 | B. | Na2O2投入水中 | ||
| C. | Al投入NaOH溶液中 | D. | 加热小苏打 |
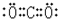 .
.