题目内容
7.锌是第四“常见”的金属,仅次于铁、铝及铜,在现代工业中对于电池的制造有不可磨灭的贡献,下列是以硫化锌精矿为原料制备单质锌的工业流程.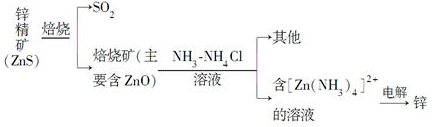
Ⅰ.(1)浸出液以硫酸锌为主,还含有 Fe3+、Fe2+、A13+、Cl-等杂质,会影响锌的电解,必须除去.净化过程如下:
①在酸性条件下,用H2O2将Fe2+氧化成Fe3+,离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
②将浸出液的pH调节为5.5左右,使 Fe3+、A13+形成沉淀而除去,可选用的最佳试剂为c
(填字母)
A.NaOH B.NH3•H2O C.Zn(OH)2D.H2SO4
③用Ag2SO4可除去Cl-,发生的离子方程式为Ag2SO4+2Cl-?2AgCl+SO42-.
④电解过程中析出锌一极的电极反应式为Zn2++2e-=Zn.
Ⅱ.烟气中的SO2可与软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的悬浊液反应制备MnSO4•H2O.
(2)已知:Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=3×10?39,pH=7.1时Mn(OH)2开始沉淀.室温下,除去MnSO4溶液中的Fe3+、Al3+(欲使其浓度小于1×10-6mol•L-1),需调节溶液pH范围为5.0<pH<7.1.
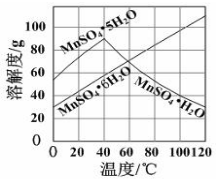
(3)由图可以看出,从MnSO4和MgSO4混合溶液中结晶MnSO4•H2O晶体,需控制结晶温度范围为高于60℃.
(4)锌锰碱性电池的总反应式为:Zn+2MnO2+2H2O═2MnO(OH)+Zn(OH)2,正极反应式为:2MnO2+H2O+2e-═Mn2O3+2OH-.
分析 硫化锌精矿焙烧得到ZnO及烟气,烟气中含有二氧化硫,ZnO焙砂用硫酸酸浸,浸出液中含有ZnSO4等,净化后得到硫酸锌溶液,再电解得到Zn.
(1)①在酸性条件下,用H2O2将Fe2+氧化成Fe3+,由电荷守恒,有氢离子参加反应,过氧化氢还原为水;
②选择的试剂能消耗氢离子,且不能引入新杂质;
③溶解平衡分别为:①Ag2SO4(s)?2Ag++SO42-,②AgCl(s)?Ag++Cl-;
④Zn2+发生还原反应得到Zn,在阴极析出;
(2)pH=7.1时Mn(OH)2开始沉淀.室温下,除去MnSO4溶液中的Fe3+、Al3+,结合Al(OH)3完全变成沉淀时的pH、Fe(OH)3完全变成沉淀时的pH分析;
(3)从MnSO4和MgSO4混合溶液中结晶MnSO4•H2O晶体,根据图上信息,高于60℃以后MnSO4•H2O的溶解度减小,而MgSO4•6H2O的溶解度增大,因此控制结晶温度范围是高于60℃;
(4)二氧化锰作正极,正极上二氧化锰得电子发生还原反应.
解答 解:(1)①在酸性条件下,用H2O2将Fe2+氧化成Fe3+,由电荷守恒,有氢离子参加反应,过氧化氢还原为水,反应离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②选择的试剂能消耗氢离子,且不能引入新杂质,加入硫酸不能消耗溶液中氢离子,NaOH、NH3•H2O、ZnO 均能消耗溶液中氢离子,但NaOH、NH3•H2O 会引入杂质离子,故选:C;
③溶解平衡分别为:①Ag2SO4(s)?2Ag++SO42-,②AgCl(s)?Ag++Cl-,①-②×2可得:Ag2SO4+2Cl-?2AgCl+SO42-,
故答案为:Ag2SO4+2Cl-?2AgCl+SO42-;
④Zn2+发生还原反应得到Zn,Zn2++2e-=Zn,
故答案为:Zn2++2e-=Zn;
(2)pH=7.1时Mn(OH)2开始沉淀.室温下,除去MnSO4溶液中的Fe3+、Al3+,氢氧化铝完全变成沉淀时的pH:Ksp[Al(OH)3]=1×10-33=c(Al3+)×c3(OH-),c(Al3+)=1×10-6mol•L-1,解得:c(OH-)=1×10-9mol•L-1,c(H+)=1×10-5mol•L-1pH=5,同理Fe(OH)3完全变成沉淀时,pH约为3.5,故pH范围是:5.0<pH<7.1,
故答案为:5.0<pH<7.1;
(3)从MnSO4和MgSO4混合溶液中结晶MnSO4•H2O晶体,根据图上信息,高于60℃以后MnSO4•H2O的溶解度减小,而MgSO4•6H2O的溶解度增大,因此控制结晶温度范围是高于60℃这样可以得到纯净的MnSO4•H2O,
故答案为:高于60℃;
(4)二氧化锰作正极,正极上二氧化锰得电子发生还原反应,电极反应式为2MnO2+H2O+2e-═Mn2O3+2OH-.
故答案为:2MnO2+H2O+2e-═Mn2O3+2OH-.
点评 本题考查较综合,涉及原电池电极反应书写、溶度积计算及混合物分离、图象分析等,综合性较强,侧重分析、计算能力的综合考查,题目难度中等.

 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案| A. | 铜、CaO、SO2 | B. | KCl、盐酸、NaOH | ||
| C. | CuSO4•5H2O、冰、乙醇 | D. | O3、CaCO3、空气 |
| A. | 反应中MnO2是氧化剂 | |
| B. | 该反应属于复分解反应 | |
| C. | KClO3在反应中失去电子 | |
| D. | 反应中每生成l mol K2MnO4,氧化剂得到2 mol电子 |
①0.5mol NH3 ②标准状况下22.4L He ③4℃9mL水 ④19.6g H3PO4.
| A. | ①④③② | B. | ④③②① | C. | ②③④① | D. | ①④②③ |
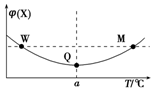 在某2L恒容密闭容器中充入2mol X(g)和1mol Y(g)发生反应:2X(g)+Y(g)?3Z(g)△H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )
在某2L恒容密闭容器中充入2mol X(g)和1mol Y(g)发生反应:2X(g)+Y(g)?3Z(g)△H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )| A. | 升高温度,平衡常数减小 | |
| B. | W、M两点Y的正反应速率相等 | |
| C. | 平衡后充入Z达到新平衡时Z的体积分数增大 | |
| D. | M点时,Y的转化率最大 |
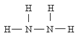 )可作为火箭发动机的燃料,NH3与NaClO反应可得到肼.
)可作为火箭发动机的燃料,NH3与NaClO反应可得到肼.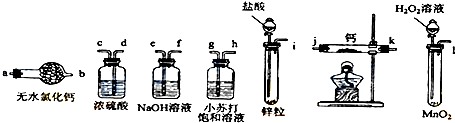
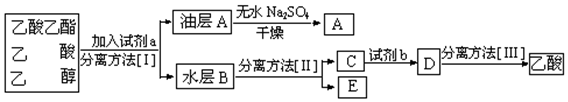
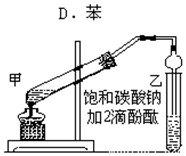 实验室制取乙酸乙酯的主要步骤如下:
实验室制取乙酸乙酯的主要步骤如下: