题目内容
16.氢气还原氧化铜:CuO+H2 $\frac{\underline{\;\;△\;\;}}{\;}$ Cu+H2O,在该反应中( )| A. | CuO作还原剂 | B. | CuO作氧化剂 | ||
| C. | 铜元素被氧化 | D. | 铜元素化合价升高 |
分析 CuO+H2 $\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O中,Cu元素的化合价降低,H元素的化合价升高,以此来解答.
解答 解:A.Cu元素的化合价降低,CuO为氧化剂,故A错误;
B.Cu元素的化合价降低,CuO为氧化剂,故B正确;
C.Cu得到电子被还原,故C错误;
D.铜元素化合价降低,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意基本概念的分析,题目难度不大.

练习册系列答案
相关题目
6.下列化学反应属于加成反应的是( )
| A. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| B. | CH2═CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl | |
| C. | CH3COOC2H5+H2O$?_{△}^{H+}$CH3COOH+C2H5OH | |
| D. | CH2═CH2+H2$→_{△}^{Ni}$CH2CH3 |
7.排布在下列各电子层上的一个电子,所具有的能量最低的是( )
| A. | K层 | B. | L层 | C. | M层 | D. | N层 |
4.下列物质中,既能和盐酸反应,又能和氢氧化钠反应的化合物是( )
| A. | 碳酸钠 | B. | 碳酸氢钠 | C. | 铝箔 | D. | 磁性氧化铁 |
11.乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )
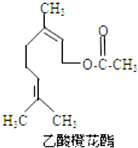

| A. | 分子式为C12H22O2 | |
| B. | 能使酸性KMnO4溶液褪色,能发生加成反应,但不能发生取代反应 | |
| C. | 1mol该有机物水解时只能消耗 1 mol NaOH | |
| D. | 1mol该有机物在一定条件下和H2反应,共消耗 H2为3mol |
1.某种塑料的结构可表示为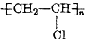 ,合成该塑料所需的原料是( )
,合成该塑料所需的原料是( )
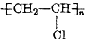 ,合成该塑料所需的原料是( )
,合成该塑料所需的原料是( )| A. | CH3Cl | B. | CH2═CHCl | C. | CH3CH2Cl | D. | CHCl═CHCl |
8.向1L、0.4mol/LH2SO4溶液中加入10.1gKNO3和9.6g铜粉,充分反应后产生的气体在标准状况下的体积为( )
| A. | 2.24L | B. | 3.36L | C. | 4.48L | D. | 5.60L |
5.关于氧气(O2)和臭氧(O3)说法正确的是( )
| A. | 互为同素异形体 | |
| B. | 二者相互转化是物理变化 | |
| C. | 同温同压下,等体积的氧气和臭氧含有相同的分子数 | |
| D. | 等物质的量的氧气和臭氧含有相同的质子数 |
6.下列关于各图的叙述,正确的是( )
| A. | 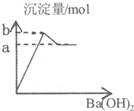 图表示向明矾溶液中滴加Ba(OH)2溶液产生沉淀的量关系曲线 | |
| B. | 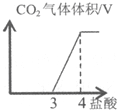 图表示向含有等物质的量的NaOH和Na2CO3溶液中加入盐酸放出CO2的关系曲线 | |
| C. | 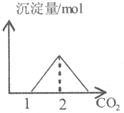 图表示向含有等物质的量的NaOH和Ca(OH)2溶液中通入CO2的产生沉淀关系曲线 | |
| D. |  图表示向NaOH溶液中滴加AlCl3溶液产生沉淀的量关系曲线 |