题目内容
5.关于氧气(O2)和臭氧(O3)说法正确的是( )| A. | 互为同素异形体 | |
| B. | 二者相互转化是物理变化 | |
| C. | 同温同压下,等体积的氧气和臭氧含有相同的分子数 | |
| D. | 等物质的量的氧气和臭氧含有相同的质子数 |
分析 A.氧气和臭氧为氧元素的不同单质;
B.氧气与臭氧之间的转化为化学变化;
C.同温同压下,等体积的气体具有相同的物质的量和分子数;
D.等物质的量的氧气和臭氧中含有氧原子的物质的量不同,则含有质子数不同.
解答 解:A.氧气(O2)和臭氧(O3)都是O元素的不同单质,二者互为同素异形体,故A正确;
B.氧气与臭氧之间的转化反应中有新物质的生成,属于化学变化,故B错误;
C.同温同压下,气体摩尔体积相同,则等体积的氧气和臭氧含有相同的分子数,故C正确;
D.等物质的量的氧气和臭氧中含有O原子的物质的量不相等,则含有质子数一定不相等,故D错误;
故选AC.
点评 本题考查了同素异形体的判断、物质的量的计算,题目难度不大,注意掌握物质的量与阿伏伽德罗常数、气体摩尔体积之间的关系,明确同素异形体的概念为解答关键,试题有利于提高学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.以下说法正确的是( )
| A. | 海洋约占地球表面积的71%,所以地球上不缺水,人类可以随意使用水资源,不必节约 | |
| B. | 海水淡化的主要方法有蒸馏法、电渗析法、离子交换法 | |
| C. | 海水淡化的各种方法中,蒸馏法的成本比较低,可用于工业生产 | |
| D. | 污水中的重金属离子无法除去,对自然界的危害是永久的,因此要关闭重金属工业 |
16.氢气还原氧化铜:CuO+H2 $\frac{\underline{\;\;△\;\;}}{\;}$ Cu+H2O,在该反应中( )
| A. | CuO作还原剂 | B. | CuO作氧化剂 | ||
| C. | 铜元素被氧化 | D. | 铜元素化合价升高 |
13.下列说法正确的是( )
| A. | 1molH2SO4与1molBa(OH)2完全中和所放出的热量为中和热 | |
| B. | 中和反应都是放热反应,盐类水解反应都是吸热反应 | |
| C. | 在101kPa1mol碳燃烧所放出的热量一定是碳的燃绕热 | |
| D. | 碳与二氧化碳的反应是放热反应,也是化合反应 |
20.在标准状况下,将0.1mol Al投入到1L0.1mol/的稀硫酸中充分反应,下列说法不正确的是( )
| A. | 该反应中Al是还原剂,稀硫酸是氧化剂 | |
| B. | 该反应中消耗Al的质量为1.8g | |
| C. | 生成2.24L H2 | |
| D. | 该反应中有0.3NA个电子发生转移 |
10.某学生对铁与水蒸气反应进行实验探究:
(1)铁粉和水蒸气反应的化学方程式3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2.
(2)操作II检验反应生成了氢气,说明水具有氧化性(填“氧化性”或“还原性”).
(3)为检验黑色固体成分,取操作IV得到的黄色溶液于两试管中,分别进行如下实验:
a.向试管1中滴加2滴KSCN溶液,溶液变红色;
b.向试管2中滴加2滴K3[Fe(CN)6]溶液,出现蓝色沉淀.
①实验a的目的是检验黄色溶液中存在Fe3+.
②由实验a、b不能判断黑色固体是磁性氧化铁,依据是操作IV中有少量气体生成,未反应完的铁也可以和盐酸反应生成Fe2+.
③该同学通过计算证实了黑色固体一定不是磁性氧化铁纯净物,n≠1.38m.(用m的表达式表示)
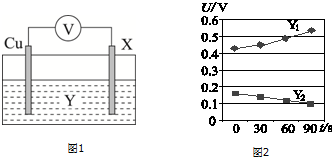
(4)资料表明:铁件与水蒸气反应,在表面生成的磁性氧化铁膜可对铁件起到防护作用.运用图1所示装置对该资料进行验证(已知:用铜片、铁件X、电解液构成原电池;氧化膜有保护时,电压会减小).
a.当Y为饱和氯化钠时,实验结果如下表:
依据U1<0.91(V),证明该条件下磁性氧化铁膜有保护作用.
b.表面有磁性氧化铁膜但存在少量缺陷的铁片作X,分别用0.1mol/LH2SO4溶液和0.1mol/L CuSO4溶液作Y进行验证实验,得到图2:
①Y2代表的溶液是0.1mol/LCuSO4溶液.
②用离子方程式解释Y1曲线变化的原因:Fe3O4+8H+=Fe2++2Fe3++4H2O..
| 操作 | 现象或结果 |
| I.取m g 铁粉,在水蒸气中加热一段时间 | 灰黑色铁粉变成黑色 |
| II.用排水集气法收集一小试管气体,移近到燃着 的酒精灯火焰 | 发出爆鸣声 |
| III.将黑色固体干燥、称量 | 得到n g 黑色固体 |
| IV.将黑色固体加入到过量的盐酸中 | 固体溶解,有少量气体生成,得到黄色溶液 |
(2)操作II检验反应生成了氢气,说明水具有氧化性(填“氧化性”或“还原性”).
(3)为检验黑色固体成分,取操作IV得到的黄色溶液于两试管中,分别进行如下实验:
a.向试管1中滴加2滴KSCN溶液,溶液变红色;
b.向试管2中滴加2滴K3[Fe(CN)6]溶液,出现蓝色沉淀.
①实验a的目的是检验黄色溶液中存在Fe3+.
②由实验a、b不能判断黑色固体是磁性氧化铁,依据是操作IV中有少量气体生成,未反应完的铁也可以和盐酸反应生成Fe2+.
③该同学通过计算证实了黑色固体一定不是磁性氧化铁纯净物,n≠1.38m.(用m的表达式表示)
(4)资料表明:铁件与水蒸气反应,在表面生成的磁性氧化铁膜可对铁件起到防护作用.运用图1所示装置对该资料进行验证(已知:用铜片、铁件X、电解液构成原电池;氧化膜有保护时,电压会减小).

a.当Y为饱和氯化钠时,实验结果如下表:
| X | U/V |
| 纯铁片 | 0.91 |
| 表面有磁性氧化铁膜的铁片 | U1 |
b.表面有磁性氧化铁膜但存在少量缺陷的铁片作X,分别用0.1mol/LH2SO4溶液和0.1mol/L CuSO4溶液作Y进行验证实验,得到图2:
①Y2代表的溶液是0.1mol/LCuSO4溶液.
②用离子方程式解释Y1曲线变化的原因:Fe3O4+8H+=Fe2++2Fe3++4H2O..
17.通常情况下,既能用浓硫酸干燥,又能用碱石灰干燥的是( )
| A. | HCl | B. | NO | C. | NH3 | D. | Cl2 |
14.下列反应的离子方程式正确的是( )
| A. | 过量CO2通入NaOH溶液中:CO2+2OH-═CO32-+H2O | |
| B. | 铜与足量浓硝酸反应:Cu+4H++2NO3-═Cu2++2NO↑+2H2O | |
| C. | 碳酸钠固体溶于水:CO32-+2H2O?H2CO3+2OH- | |
| D. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ |
15.第3周期某元素的原子,其最外层3p亚层上有一个未成对电子,则关于该元素的描述正确的是( )
| A. | 该元素最高价氧化物的水化物肯定是一种强酸 | |
| B. | 该元素单质肯定是一种黄绿色的气体 | |
| C. | 该元素的最高价氧化物肯定能与强碱反应 | |
| D. | 该元素的原子半径在同周期中肯定是最小的(稀有气体元素除外) |