题目内容
17.有机物M可从酸牛奶中提取.已知纯净的M为无色黏稠液体,易溶于水.为研究M的组成与结构,进行了如下实验:| 实验步骤 | 解释或实验结论 |
| (1)称取M 4.5g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空:(1)M的摩尔质量为:90g/mol. |
| (2)将此4.5g M在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g | (2)M的分子式为:C3H6O3. |
| (3)通过M的红外光谱图发现该分子中既有羟基,还有羧基(--COOH) | (3)写出M中含有官能团羟基的电子式: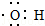 |
(4)M的核磁共振氢谱如图: | (4)M中含有4种氢原子. |
(5)综上所述,M的结构简式为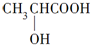 . . | |
分析 (1)相同条件下气体密度与摩尔质量成正比,据此可计算出M的摩尔质量;
(2)浓硫酸增重的为水的质量,碱石灰增重的为二氧化碳的质量,根据质量守恒定律确定其分子式;
(3)羟基中含有1个O-H键,氧原子最外层含有7个电子,据此写出羟基的电子式;
(4)核磁共振氢谱中含有几组吸收峰,则M分子中含有几种H原子;
(5)根据M的分子式、含有官能团及H原子数目确定M的结构简式.
解答 解:(1)称取M 4.5g,升温使其汽化,测其密度是相同条件下H2的45倍,则M的摩尔质量为:2g/mol×45=90g/mol,
故答案吴娜:90g/mol;
(2)将此4.5g M在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g,说明4.5gM完全燃烧生成水的质量为2.7g,其物质的量为:$\frac{2.7g}{18g/mol}$=0.15mol,生成二氧化碳的质量为6.6g,其物质的量为:$\frac{6.6g}{44g/mol}$=0.15mol,
4.5gM的物质的量为:$\frac{4.5g}{90g/mol}$=0.05mol,则M分子中含有C、H原子的数目分别为:N(C)=$\frac{0.15mol}{0.05mol}$=3、N(H)=$\frac{0.15mol×2}{0.05mol}$=6,
M分子中含有C、H的总原子量为:12×3+1×6=42<90,说明M分子中还含有氧原子,含有氧原子数目为:N(O)=$\frac{90-42}{16}$=3,
所以M的分子式为:C3H6O3,
故答案为:C3H6O3;
(3)羟基为中性原子团,其电子式为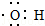 ,
,
故答案为: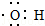 ;
;
(4)根据M的核磁共振氢谱可知,吸收峰数目为4,则M分子中含有4种H原子,
故答案为:4;
(5)根据以上分析可知,M的分子式为C3H6O3,含有1个羟基和1个羧基,且M分子中含有4种H原子,则M的结构简式为: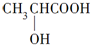 ,
,
故答案为: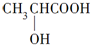 .
.
点评 本题考查了有机物结构与性质,题目难度中等,明确常见有机物结构与性质为解答结构,注意掌握守恒思想在确定有机物分子式中的应用方法,试题培养了学生的分析能力及化学计算能力.

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案| A. | 0.1mol/L | B. | 0.5mol/L | C. | 1mol/L | D. | 2mol/L |
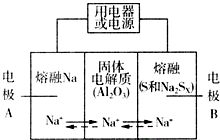 钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:Na2SX$?_{放电}^{充电}$ 2Na+XS (3<X<5)
钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:Na2SX$?_{放电}^{充电}$ 2Na+XS (3<X<5)| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
A.100℃以下 B.100℃~300℃
C.300℃~350℃D.350℃~2050℃
(2)关于钠硫电池,下列说法正确的是AD(填字母序号).
A.放电时,电极A为负极
B.放电时,Na+的移动方向为从B到A
C.充电时,电极A应连接电源的正极
D.充电时电极B的电极反应式为SX2--2e-=xS
(3)25℃时,若用钠硫电池作为电源电解500mL 0.2mol•L-1 NaCl溶液,当溶液的pH变为l3时(忽略电解前后溶液的体积变化),电路中通过的电子的物质的量为0.05mol,钠硫电池两极的反应物的质量差为2.3 g.(假设电解前钠硫电池两极的反应物质量相等)
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
| A. | 摩尔是一种国际基本物理量 | |
| B. | 1mol氢气的质量为1g | |
| C. | 在同温同压下,相同体积的任何气体所含分子数相同 | |
| D. | 标准状况下,1mol任何物质的体积都约为22.4L |
 H2PO4-+H+.
H2PO4-+H+.