题目内容
2.相对分子质量为43的烷基取代甲苯苯环上的一个氢原子,所得产物的数目为( )| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
分析 根据烷基式量为43的确定烷基,再判断可能的烷基异构情况,利用等效H判断甲苯苯环上的H原子种类有3种,据此判断.
解答 解:烷基组成通式为CnH2n+1,烷基式量为43,所以14n+1=43,解得n=3,所以烷基为-C3H7,
当为正丙基,甲苯苯环上的H原子种类有3种,所以有3种同分异构体.
当为异丙基,甲苯苯环上的H原子种类有3种,所以有3种同分异构体.
故该芳香烃产物的种类数为6种.
故选D.
点评 考查同分异构体的书写,难度中等,关键根据烷基式量为43的确定烷基,判断可能的烷基异构情况.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
1.已知金刚石在一定条件下转化为石墨是放热的,则金刚石和石墨比较,能量“贮存”高的是( )
| A. | 石墨 | B. | 金刚石 | C. | 一样高 | D. | 无法判断 |
13.下列实验事实或结论正确的是( )
| A. | 二氧化硫气体通入硝酸钡溶液,生成白色BaSO4沉淀 | |
| B. | 氨气的水溶液可以导电,所以氨气是电解质 | |
| C. | 酸性高锰酸钾溶液中通入二氧化硫气体,溶液褪色,证明二氧化硫有漂白性 | |
| D. | 硝酸具有挥发性,所以硝酸不稳定 |
10.下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在③~⑦元素中,原子半径最大的是Na,其离子的原子结构示意图为
(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3;
(3)写出物质的电子式:①的氢化物 .
.
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |

(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3;
(3)写出物质的电子式:①的氢化物
 .
.
17.有机物M可从酸牛奶中提取.已知纯净的M为无色黏稠液体,易溶于水.为研究M的组成与结构,进行了如下实验:
| 实验步骤 | 解释或实验结论 |
| (1)称取M 4.5g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空:(1)M的摩尔质量为:90g/mol. |
| (2)将此4.5g M在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g | (2)M的分子式为:C3H6O3. |
| (3)通过M的红外光谱图发现该分子中既有羟基,还有羧基(--COOH) | (3)写出M中含有官能团羟基的电子式: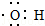 |
(4)M的核磁共振氢谱如图: | (4)M中含有4种氢原子. |
(5)综上所述,M的结构简式为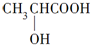 . . | |
7.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 14g乙烯、丙烯、丁烯的混合气体中所含原子数为3NA | |
| B. | 28g乙烯所含共用电子对数目为5NA | |
| C. | 标准状况下,11.2 L氯仿所含分子数为0.5 NA | |
| D. | 46g乙醇中含有C-H键数目为6NA |
11.二氧化锆是重要的耐高温材料、陶瓷绝缘材料.以锆英砂(主要成分为ZrSiO4,还含有少量Fe2O3、Al2O3、SiO2等杂货)为原料制备二氧化锆(ZrO2)的工艺流程如图所示.
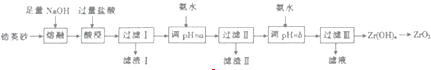
已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO2,Na2ZrO2与酸反应生成ZrO2+
②部分离子在实验条件下开始沉淀和完全沉淀时的pH如表?
(l)经熔融后,锆英砂中Zr元素以Na2ZrO3(写化学式)形式存在,写出酸浸时生成Al3+、Fe3+的离子方程式:Fe2O3+6H+=Fe3++3H2O,AlO2-+4H+=Al3++2H2O
(2)滤渣I的主要成分的名称为硅酸
(3)向过滤Ⅰ所得溶液中加氨水调pH=a,其目的是除去Fe3+、Al3+
(4)向过滤Ⅲ所得溶液中加入CaCO2粉末并加热,可得CO2和另一种气体,该反应的离子方程式为2NH4++CaCO3$\frac{\underline{\;\;△\;\;}}{\;}$Ca2++2NH3↑+CO2↑+H2O.

已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO2,Na2ZrO2与酸反应生成ZrO2+
②部分离子在实验条件下开始沉淀和完全沉淀时的pH如表?
| 离子 | Fe3+ | AP+ | ZrO2+ |
| 开始沉淀pH | 1.9 | 3.3 | 6.2 |
| 完仝沉淀pH | 3.2 | 5.2 | 8.0 |
(2)滤渣I的主要成分的名称为硅酸
(3)向过滤Ⅰ所得溶液中加氨水调pH=a,其目的是除去Fe3+、Al3+
(4)向过滤Ⅲ所得溶液中加入CaCO2粉末并加热,可得CO2和另一种气体,该反应的离子方程式为2NH4++CaCO3$\frac{\underline{\;\;△\;\;}}{\;}$Ca2++2NH3↑+CO2↑+H2O.
12.下列各组中的两种物质互为同分异构体的是( )
| A. | 乙烷和乙酸 | B. | 淀粉和纤维素 | ||
| C. | CH3CH2CH2CH3和CH3CH2CH3 | D. | 乙醇和二甲醚 |
