题目内容
16.将4gNaOH固体溶于水配成100mL溶液,该溶液中NaOH的物质的量浓度为( )| A. | 0.1mol/L | B. | 0.5mol/L | C. | 1mol/L | D. | 2mol/L |
分析 将4gNaOH固体溶于水配成100mL溶液,先根据n=$\frac{m}{M}$计算出4g氢氧化钠的物质的量,然后根据c=$\frac{n}{V}$计算出所得溶液的物质的量浓度.
解答 解:4g NaOH的物质的量为:n(NaOH)=$\frac{4g}{40g/mol}$=0.1mol,
0.1mol NaOH配成100mL溶液,所得溶液的物质的量浓度为:c(NaOH)=$\frac{0.1mol}{0.1L}$=1mol/L,
故选C.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量与摩尔质量、物质的量浓度之间的关系为解答关键,注意掌握物质的量浓度的概念及表达式,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列说法正确的是( )
| A. | 石蜡油分解产生的气态产物中不含有不饱和烃 | |
| B. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 | |
| C. | 油脂是种高级脂肪酸甘油酯,其中植物油通过氢化可以变成脂肪 | |
| D. | 苯与浓硝酸、浓硫酸混合,加强热以制备硝基苯 |
11.下列说法正确的是( )
| A. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| B. | 工艺师利用盐酸刻蚀石英制作艺术品 | |
| C. | 硅是人类将太阳能转换为电能的常用材料 | |
| D. | 由粗硅制备单晶硅不涉及氧化还原 |
1.已知金刚石在一定条件下转化为石墨是放热的,则金刚石和石墨比较,能量“贮存”高的是( )
| A. | 石墨 | B. | 金刚石 | C. | 一样高 | D. | 无法判断 |
8.下列说法不正确的是( )
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口下沿处 | |
| C. | 蒸发结晶时应将溶液蒸干 | |
| D. | 能用CCl4从碘水中萃取碘是由于CCl4与H2O互不相溶且碘在CCl4中溶解度比在水中的大 |
5.短周期主族元素X、Y、Z、W的原子序数依次增大.X、Y、Z、W原子的最外层电子数之和为18,X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构.下列说法正确的是( )
| A. | Y分别与Z、W形成的化合物中化学键类型不相同 | |
| B. | 单质的沸点:Y>Z | |
| C. | X、Y、Z三种元素不可能形成离子化合物 | |
| D. | X的最高价氧化物对应的水化物的酸性比W的强 |
17.有机物M可从酸牛奶中提取.已知纯净的M为无色黏稠液体,易溶于水.为研究M的组成与结构,进行了如下实验:
| 实验步骤 | 解释或实验结论 |
| (1)称取M 4.5g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空:(1)M的摩尔质量为:90g/mol. |
| (2)将此4.5g M在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g | (2)M的分子式为:C3H6O3. |
| (3)通过M的红外光谱图发现该分子中既有羟基,还有羧基(--COOH) | (3)写出M中含有官能团羟基的电子式: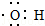 |
(4)M的核磁共振氢谱如图: | (4)M中含有4种氢原子. |
(5)综上所述,M的结构简式为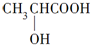 . . | |