题目内容
8.已知X、Y、Z、W是短周期元素中的四种非金属元素,它们的原子序数依次增大. X元素的原子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍.(1)请写出Z在元素周期表中的位置为第二周期、第VA族.
(2)气体分子(YZ)2的电子式为
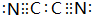 .
.(3)由X、Y、Z、W四种元素可组成酸式盐,该化合物的水溶液与足量NaOH溶液在加热条件下反应的离子方程式为NH4++HCO3-+2OH-=NH3↑+2H2O+CO32-.
(4)在一定条件下,由X单质与Z单质可化合生成E,工业上用E检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质Z生成,写出化学方程式8NH3+3Cl2=6NH4Cl+N2.该反应中被氧化的E与参与反应的E的质量之比1:4.
分析 X、Y、Z、W是短周期中四种非金属元素,它们的原子序数依次增大,X元素原子形成的离子就是一个质子,则X是H元素;Y原子的最外层电子数是内层电子数的2倍,最外层电子不能超过8,只能有2个电子层,最外层电子数为4,则Y是C元素;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,且Z的原子序数小于W,所以Z是N元素,W是O元素,据此解答.
解答 解:X、Y、Z、W是短周期中四种非金属元素,它们的原子序数依次增大,X元素原子形成的离子就是一个质子,则X是H元素;Y原子的最外层电子数是内层电子数的2倍,最外层电子不能超过8,只能有2个电子层,最外层电子数为4,则Y是C元素;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,且Z的原子序数小于W,所以Z是N元素,W是O元素.
(1)Z为氮元素,N有2个电子层,最外层5个电子,处于第二周期第ⅤA族,故答案为:二、ⅤA;
(2)气体分子(CN)2的电子式为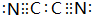 ,故答案为:
,故答案为: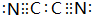 ;
;
(3)H、C、N、O四种元素可组成酸式盐NH4HCO3,碳酸氢铵与足量浓NaOH溶液反应生成碳酸钠、氨气与水,反应离子方程式为:NH4++HCO3-+2OH-=NH3↑+2H2O+CO32-,
故答案为:NH4++HCO3-+2OH-=NH3↑+2H2O+CO32-;
(4)工业上用E检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质氮气生成,故E为NH3,化学方程式为:8NH3+3Cl2=6NH4Cl+N2,该反应中被氧化的NH3与参与反应的NH3的质量之比为2:8=1:4,
故答案为:8NH3+3Cl2=6NH4Cl+N2;1:4.
点评 本题考查结构性质位置关系应用,涉及电子式、分子结构、离子方程式、氧化还原反应等,正确推断元素是解本题关键,难度中等,(3)中注意不能写成NH3.H2O,为易错点.

| A. | 盐酸 | B. | KHS溶液 | C. | NaOH溶液 | D. | Na2S溶液 |
所用酸性KMnO4溶液的浓度可选择0.010mol•L-1、0.0010mol•L-1,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液(0.10mol•L-1)的用量均为2mL.
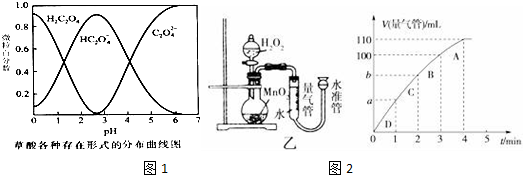
(1)已知草酸溶液中各种微粒存在形式的分布曲线图如图1,请写出KMnO4酸性溶液与H2C2O4溶液反应的离子方程式2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
(2)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 催化剂的用量/g | 酸性KMnO4溶液的浓度/mol•L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.010 | a.实验①和②探究酸性KMnO4溶液的浓度对该反应速率的影响; b.实验①和③ 探究温度对反应速率的影响; c.实验①和④ 探究催化剂对反应速率的影响. |
| ② | ||||
| ③ | 0.010 | |||
| ④ |
| 实验编号 | 溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| Ⅰ | 14.0 | 13.0 | 11.0 |
| Ⅱ | 6.5 | 6.7 | 6.8 |
②该同学分析上述数据后得出“当其他条件相同的情况下,酸性KMnO4溶液的浓度越小,所需要的时间就越短,亦即其反应速率越快”的结论,你认为是否正确否(填“是”或“否”).他认为不用经过计算,直接根据表中褪色时间的长短就可以判断浓度大小与反应速率的关系,你认为是否可行否(填“是”或“否”),若不可行(若认为可行则不填),请设计可以直接通过观察褪色时间的长短来判断的改进方案:取过量的体积相同、浓度不同的草酸溶液,分别同时与体积相同、浓度相同的酸性高锰酸钾溶液反应
(4)该反应的催化剂选择MnCl2还是MnSO4并简述选择的理由:MnSO4,如选用MnCl2,则酸性高锰酸钾会与Cl-反应,而且引入了Cl-无法证明是Mn2+起了催化作用
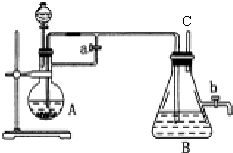
(5)化学催化剂有很多,在生产和科技领域起到重大作用.探究小组又利用乙装置探究MnO2对H2O2分解的催化效果.将50mL H2O2一次性加入盛有0.10mol MnO2粉末的烧瓶中,测得标准状况下由量气管读出气体的体积[V(量气管)/mL]和时间(t/min)的关系如图2所示.
①实验时放出气体的总体积是110mL.
②b小于(填“大于”“小于”或“等于”)90mL.
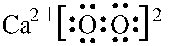 ;加热过氧化钙可分解生成CaO和O2,该反应的化学方程式为2CaO2$\frac{\underline{\;\;△\;\;}}{\;}$2CaO+O2↑.
;加热过氧化钙可分解生成CaO和O2,该反应的化学方程式为2CaO2$\frac{\underline{\;\;△\;\;}}{\;}$2CaO+O2↑.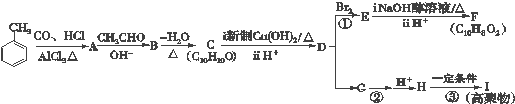
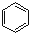 $→_{AlCl_{3}△}^{CO、HCl}$
$→_{AlCl_{3}△}^{CO、HCl}$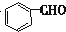
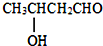 $→_{△}^{-H_{2}O}$CH3CH=CHCHO
$→_{△}^{-H_{2}O}$CH3CH=CHCHO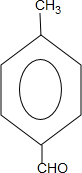 .
. +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O. $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +nH2O.
+nH2O.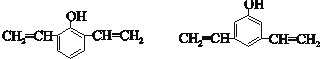 .
.