题目内容
12.下列有机化合物转化关系如图所示: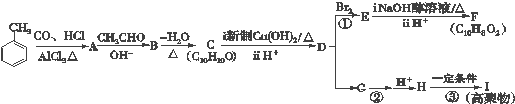
已知:
(1)
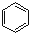 $→_{AlCl_{3}△}^{CO、HCl}$
$→_{AlCl_{3}△}^{CO、HCl}$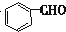
(2)CH3CHO+CH3CHO$\stackrel{OH-}{→}$
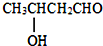 $→_{△}^{-H_{2}O}$CH3CH=CHCHO
$→_{△}^{-H_{2}O}$CH3CH=CHCHO其中化合物A苯环上的一氯代物只有两种.请回答下列问题:
(1)写出A的结构简式
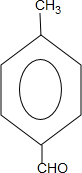 .
.(2)B中含有的官能团的名称羟基和醛基.
(3)①、③的反应类型分别为加成反应、缩聚反应;化合物F的核磁共振氢谱显示有4个峰.
(4)写出C与新制Cu(OH)2反应的化学方程式
 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O.(5)已知两分子H能形成六元环酯,写出反应③的化学方程式n
 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +nH2O.
+nH2O.(6)化合物C有多种同分异构体,请写出其中满足下列条件的所有同分异构体的结构简式
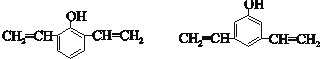 .
.①遇氯化铁溶液显紫色;②苯环上有三个取代基;③苯环上的一氯取代物只有两种.
分析 据已知信息和化合物A苯环上的一氯代物只有两种可知A为 ,A与CH3CHO发生信息所示的羟醛缩合反应生成B,B为
,A与CH3CHO发生信息所示的羟醛缩合反应生成B,B为 ,B发生消去反应生成C,C为
,B发生消去反应生成C,C为 ,C与新制氢氧化铜反应,醛基被氧化为羧基,D为
,C与新制氢氧化铜反应,醛基被氧化为羧基,D为 ,D与溴水发生加成反应后,在NaOH的乙醇溶液中发生消去反应酸化后生成F,F为
,D与溴水发生加成反应后,在NaOH的乙醇溶液中发生消去反应酸化后生成F,F为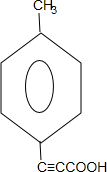 ,两分子H能形成六元环酯,说明H为
,两分子H能形成六元环酯,说明H为 ,D→G是
,D→G是 与HX的加成反应,再在NaOH的水溶液中水解生成H,H发生缩聚反应生成I为
与HX的加成反应,再在NaOH的水溶液中水解生成H,H发生缩聚反应生成I为 ,据此分析.
,据此分析.
解答 解:据已知信息和化合物A苯环上的一氯代物只有两种可知A为 ,A与CH3CHO发生信息所示的羟醛缩合反应生成B,B为
,A与CH3CHO发生信息所示的羟醛缩合反应生成B,B为 ,B发生消去反应生成C,C为
,B发生消去反应生成C,C为 ,C与新制氢氧化铜反应,醛基被氧化为羧基,D为
,C与新制氢氧化铜反应,醛基被氧化为羧基,D为 ,D与溴水发生加成反应后,在NaOH的乙醇溶液中发生消去反应酸化后生成F,F为
,D与溴水发生加成反应后,在NaOH的乙醇溶液中发生消去反应酸化后生成F,F为 ,两分子H能形成六元环酯,说明H为
,两分子H能形成六元环酯,说明H为 ,D→G是
,D→G是 与HX的加成反应,再在NaOH的水溶液中水解生成H,H发生缩聚反应生成I为
与HX的加成反应,再在NaOH的水溶液中水解生成H,H发生缩聚反应生成I为 ,
,
(1)据已知信息和化合物A苯环上的一氯代物只有两种可知A为 ,故答案为:
,故答案为: ;
;
(2)B为 ,其含有羟基和醛基两种官能团,故答案为:羟基和醛基;
,其含有羟基和醛基两种官能团,故答案为:羟基和醛基;
(3)D与溴水发生加成反应生成E,H发生缩聚反应生成I,F为 ,F中有4中氢原子,所以核磁共振氢谱显示有4个峰,
,F中有4中氢原子,所以核磁共振氢谱显示有4个峰,
故答案为:加成反应、缩聚反应;4;
(4)C为 ,C与新制氢氧化铜反应,醛基被氧化为羧基,D为
,C与新制氢氧化铜反应,醛基被氧化为羧基,D为 ,化学方程式为:
,化学方程式为: +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O,
+Cu2O↓+2H2O,
故答案为: +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O;
+Cu2O↓+2H2O;
(5)两分子H能形成六元环酯,说明H为 ,H通过缩聚反应生成高聚物I的方程式为n
,H通过缩聚反应生成高聚物I的方程式为n $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +nH2O,
+nH2O,
故答案为:n $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +nH2O;
+nH2O;
(6)C为 ,其同分异构体①遇氯化铁溶液显紫色,说明有酚羟基,②苯环上有三个取代基 ③苯环上的一氯取代物只有两种,说明有两个取代基相同,为
,其同分异构体①遇氯化铁溶液显紫色,说明有酚羟基,②苯环上有三个取代基 ③苯环上的一氯取代物只有两种,说明有两个取代基相同,为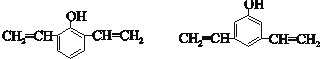 ,
,
故答案为: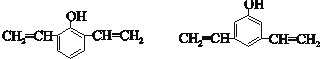 .
.
点评 本题考查有机物推断、有机反应类型、官能团判断、有机方程式书写等,难度不大,涉及炔、烯烃的性质与转化,注意对基础知识的理解掌握.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 可用灼烧的方法区别丝绸与棉布 | |
| B. | 可用焰色反应区别硫酸钠和硫酸钾 | |
| C. | 可用结晶的方法分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃) | |
| D. | 可用分液的方法分离汽油和水 |
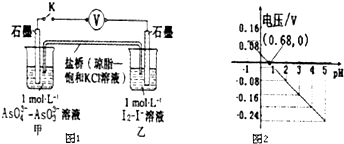
| A. | 调节pH可以改变反应的方向 | |
| B. | pH=0.68 时,反应处于平衡状态 | |
| C. | pH=5 时,负极电极反应式为2I--2e-═I2 | |
| D. | pH>0.68时,氧化性I2>AsO${\;}_{4}^{3-}$ |
 某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液.下列说法正确的是( )
某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液.下列说法正确的是( )| A. | a电极上发生的反应为:MnO4-+8H++5e-═Mn2++4H2O | |
| B. | 外电路电子的流向是从a到b | |
| C. | 电池工作时,盐桥中的SO42-移向甲烧杯 | |
| D. | b电极上发生还原反应 |
| A. | 常温下,用pH计测定0.1mol/L的甲酸钠溶液pH为13 | |
| B. | 向饱和醋酸钠溶液中添加0.1mol/L的碳酸钠溶液产生了无色气体 | |
| C. | 少量Mg(OH)2沉淀中加入氯化铵浓溶液可以观其察到白色沉淀溶解 | |
| D. | 向2ml 1mol/L的NaOH溶液中加入3滴 1mol/L MgCl2溶液,再加入3 滴1mol/L FeCl3溶液可以证明Mg(OH)2沉淀转变成Fe(OH)3沉淀 |
| 元素 | 结构特点及元素、单质、化合物的性质 |
| X | 气态氢化物与最高价氧化物对应水化物可以化合成盐 |
| Y | 原子中s电子数与p电子数相同,且p电子的能量最高 |
| Z | 单质在空气中燃烧产生黄色火焰,生成黄色粉末 |
| W | 最外层电子排布(n+1)sn(n+1)pn-1 |
| T | 单质升华可以产生紫色的烟 |
(2)Z单质在空气中燃烧生成黄色粉末,写出该物质的电子式
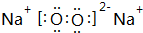 ;已知w 的氯化物在177.8°C时会发生升华现象,由此可以判断它的晶体类型为分子晶体.
;已知w 的氯化物在177.8°C时会发生升华现象,由此可以判断它的晶体类型为分子晶体.(3)W的最高价氧化物对应水化物可以与X、Z的最高价氧化物对应水化物反应,写出反 应的离子方程式:Al(OH)3+3H+=Al3++3H2O,Al(OH)3+OH-=AlO2-+2H2O.
(4)一种元素有多种可变价态,一般高价氧化物对应水化物成酸,低价氧化物对应水化物成碱.Y、T可形成多种化合物,其中T元素的化合价为+3、+5时,形成的化合物的化学式为AB.
A.T2Y4 B.T4Y9 C.T6Y10 D.T2Y3.
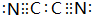 .
.
