题目内容
20.下列关于物质性质变化的比较,不正确的是( )| A. | 非金属性强弱:I>Br>Cl | B. | 原子半径大小:Na>P>S | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 金属性强弱:Na>Mg>Al |
分析 A.同一主族元素,元素的非金属性随着原子序数增大而减弱;
B.同一周期元素,原子半径随着原子序数增大而减小;
C.元素的金属性越强,其最高价氧化物的水化物碱性越强;
D.同一周期元素,元素的金属性随着原子序数增大而减弱.
解答 解:A.同一主族元素,元素的非金属性随着原子序数增大而减弱,所以非金属性强弱:I<Br<Cl,故A错误;
B.同一周期元素,原子半径随着原子序数增大而减小,所以原子半径大小:Na>P>S,故B正确;
C.元素的金属性越强,其最高价氧化物的水化物碱性越强,金属性K>Na>Li,所以碱性强弱:KOH>NaOH>LiOH,故C正确;
D.同一周期元素,元素的金属性随着原子序数增大而减弱,所以金属性强弱:Na>Mg>Al,故D正确;
故选A.
点评 本题考查元素周期律,为高频考点,明确同一周期、同一主族元素性质递变规律是解本题关键,知道金属性、非金属性强弱的判断方法,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
10.短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是( )
| A. | 元素X的简单气态氢化物的热稳定性比W的弱 | |
| B. | 元素W的最高价氧化物对应水化物的酸性比Z的弱 | |
| C. | 化合物YX、ZX2、WX3中化学键的类型相同 | |
| D. | 原子半径的大小顺序:Y>Z>W>X |
8.下列叙述正确的是( )
| A. | 用标准的盐酸溶液滴定含甲基橙的氢氧化钠溶液,终点时溶液由黄色变成橙色 | |
| B. | 将二氧化硫通入氯化钡溶液中产生白色沉淀,再滴加稀硝酸沉淀不消失 | |
| C. | 向葡萄糖溶液中加入新制氢氧化铜,加热至沸腾,静置后上层溶液呈红色 | |
| D. | 海水提取溴的过程不发生氧化还原反应 |
15.足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与3.2g O2混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入NaOH溶液至Cu2+恰好完全沉淀,则消耗溶液中NaOH的质量是( )
| A. | 16g | B. | 32g | C. | 64g | D. | 无法计算 |
5.下列说法中不正确的是( )
| A. | 共价化合物中一定不含有离子键,离子化合物中可能含有共价键 | |
| B. | 充电电池的化学反应原理是氧化还原反应 | |
| C. | 一定条件下,将1 mol N2与3 mol H2充入密闭容器中充分反应可生成2 mol NH3 | |
| D. | 质子数相同、电子数也相同的两种微粒,不可能是一种分子和一种离子 |
12.下列不属于晶体特点的是( )
| A. | 有固定的几何外形 | B. | 一定有各向异性 | ||
| C. | 一定有固定的熔点 | D. | 一定是无色透明的固体 |
9.实验室有几瓶标签脱落的无色液体:己烯、苯、四氯化碳、氢氧化钠溶液、苯酚溶液、碘化钾溶液,只用一种试剂即可鉴别,则该试剂可能是( )
| A. | 高锰酸钾 | B. | 氯化铁 | C. | 浓溴水 | D. | 水 |
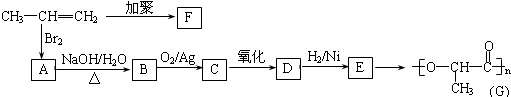
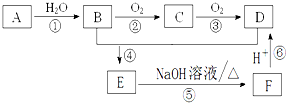 已知:A是石油裂解气的主要成份且A的产量通常用来衡量一个国家的石油化工水平;请回答下列问题:
已知:A是石油裂解气的主要成份且A的产量通常用来衡量一个国家的石油化工水平;请回答下列问题: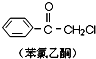 ,则苯氯乙酮不可能具有的化学性质是ce(填字母序号).
,则苯氯乙酮不可能具有的化学性质是ce(填字母序号).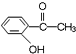 乙:
乙: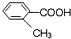 丙:
丙: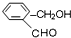
 .
. .
.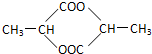 .
.