题目内容
12.下列不属于晶体特点的是( )| A. | 有固定的几何外形 | B. | 一定有各向异性 | ||
| C. | 一定有固定的熔点 | D. | 一定是无色透明的固体 |
分析 晶体具有自范性、各向异性和固定的熔沸点,晶体不一定是无色透明的固体,以此解答.
解答 解:晶体(单晶体和多晶体)和非晶体的区别:(1)单晶体有整齐规则的几何外形;(2)晶体有固定的熔点;(3)单晶体有各向异性的特点,晶体不一定是无色透明的固体,例如晶体不一定是无色透明的固体,如硫酸铜晶体为蓝色,但有些非晶体无色透明,如玻璃,
故选D.
点评 本题考查晶体特点,注意把握晶体的性质,题目难度不大,学习中注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.关于有机物的下列说法,不正确的是( )
| A. | 石油裂解能得到乙烯,乙烯是生产聚乙烯的原料 | |
| B. | 丙烷、丙烯都属于烃,都有同分异构体 | |
| C. | 葡萄糖可转化为乙醇,乙醇氧化可得到乙醛 | |
| D. | 煤干馏为化学变化,石油分馏是物理变化 |
3.设NA是阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L乙醇中含有的氧原子数为NA | |
| B. | 标准状况下,22.4L37Cl2中所含中子数为40NA | |
| C. | 将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NA个Fe3+ | |
| D. | 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有OH-数目为0.2NA |
20.下列关于物质性质变化的比较,不正确的是( )
| A. | 非金属性强弱:I>Br>Cl | B. | 原子半径大小:Na>P>S | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 金属性强弱:Na>Mg>Al |
4.向某溶液中加入BaCl2溶液,生成白色沉淀,加入稀硝酸沉淀不消失,则下列关于溶液中所含离子的推断中正确的( )
| A. | 一定含有SO42- | B. | 含有SO42- 或Ag+ | ||
| C. | 含有SO42- 或Ag+ 或SO32- | D. | 可能含有SO32- 或CO32- |
2.2003年诺贝尔化学奖授予两位美国科学家,其中一位是阿格雷(Pete Agre),表彰他最先发现并表征了细胞膜上的水通道蛋白质,并把这种蛋白质暂命名为:CHIP28,下列关于CHIP28的说法中正确的是( )
| A. | 这种蛋白质为人工合成的高分子化合物 | |
| B. | 这种蛋白质遇到HgCl2的浓溶液将发生盐析 | |
| C. | 这种蛋白质能完全水解生成单糖分子 | |
| D. | 这种蛋白质分子中存在“-CONH-”的结构 |
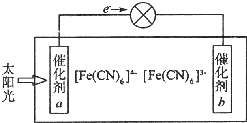 铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题.
铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题.
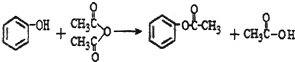
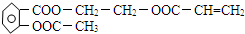 .
.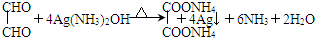
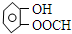 (或间、对位)
(或间、对位)