题目内容
16.在下列变化过程中,既有离子键被破坏又有共价键被破坏的是( )| A. | 将CO2溶于水中 | B. | Na2O2溶于水中 | C. | 将SO3溶于水中 | D. | NaHSO4溶于水中 |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,化学变化中及电解质中的电离中有化学键的断裂,以此来解答.
解答 解:A.将CO2溶于水中,生成碳酸,只有共价键的断裂和生成,故A不选;
B.Na2O2溶于水中,生成NaOH和氧气,既有离子键被破坏又有共价键被破坏,故B选;
C.将SO3溶于水中,生成硫酸,只有共价键的断裂和生成,故C不选;
D.NaHSO4溶于水中,电离生成钠离子、氢离子、硫酸根离子,既有离子键被破坏又有共价键被破坏,故D选;
故选BD.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断为解答的关键,侧重分析与应用能力的考查,注意化学变化及电离中的化学键变化,题目难度不大.

练习册系列答案
相关题目
6.氢化铵与氯化铵结构相似,下列叙述中不正确的是( )
| A. | NH4H的电子式为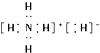 | |
| B. | 1molNH5中含有5NA个N-H键(NA表示阿伏伽德罗常数的数值) | |
| C. | NH4H中的H-半径比锂离子半径大 | |
| D. | NH4H晶体既有共价键又有离子键 |
7.化学与生产生活密切相关,下列说法不正确的是( )
| A. | 液氨汽化时吸热,可作制冷剂 | |
| B. | 氧化铝熔点高,可作耐火材料 | |
| C. | 利用酒精沸点较低,可作消毒杀菌剂 | |
| D. | 利用CO2合成的聚碳酸酯能水解,可作降解塑料 |
11.下列关于电解质导电性的说法中,正确的是( )
| A. | 电解质溶液的导电性强弱是由浓度决定的 | |
| B. | 弱电解质和强电解质的导电,都是由带电离子的定向移动引起的 | |
| C. | 强电解质溶液导电能力强,弱电解质溶液导电能力弱 | |
| D. | 导电性强的溶液中的自由移动离子数目一定比导电性弱的溶液中的自由移动离子数目多 |
1.下列分子中每个原子的最外层都满足8电子的是( )
| A. | F2 | B. | H2O | C. | PCl3 | D. | SO2 |
9.下列各溶液中,Cl-浓度最大的是( )
| A. | 2 L 0.1 mol•L-1的AlCl3溶液 | B. | 1 L 0.1 mol•L-1的FeCl2溶液 | ||
| C. | 1 L 1 mol•L-1的NaCl溶液 | D. | 1 L 2 mol•L-1的KClO3溶液 |
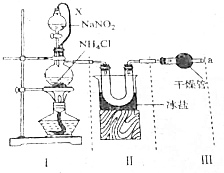 氮气、氨及铵盐用途非常广泛.回答下列问题:
氮气、氨及铵盐用途非常广泛.回答下列问题: