题目内容
9.下列各溶液中,Cl-浓度最大的是( )| A. | 2 L 0.1 mol•L-1的AlCl3溶液 | B. | 1 L 0.1 mol•L-1的FeCl2溶液 | ||
| C. | 1 L 1 mol•L-1的NaCl溶液 | D. | 1 L 2 mol•L-1的KClO3溶液 |
分析 根据溶液中不水解的离子的物质的量浓度=溶质的物质的量浓度×化学式中离子的个数,与溶液的体积无关,据此分析解答.
解答 解:A.2 L 0.1 mol•L-1的AlCl3溶液,氯离子浓度为0.1mol/L×3=0.3mol/L;
B.1 L 0.1 mol•L-1的FeCl2溶液,氯离子浓度为0.1mol/L×2=0.2mol/L;
C.1 L 1 mol•L-1的NaCl溶液,氯离子浓度为1mol/L×1=1mol/L;
D.氯酸钾溶液中不含有氯离子;
Cl-的浓度最大的是1mol/L,
故选:C.
点评 本题考查物质的量浓度的计算与理解,题目难度不大,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.

练习册系列答案
相关题目
16.在下列变化过程中,既有离子键被破坏又有共价键被破坏的是( )
| A. | 将CO2溶于水中 | B. | Na2O2溶于水中 | C. | 将SO3溶于水中 | D. | NaHSO4溶于水中 |
20.下列物质中,既含有离子键,又含有共价键的是( )
| A. | H2O | B. | MgCl2 | C. | NaOH | D. | CH3COOH |
4.下列各组性质比较中,正确的是( )
①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Mg(OH)2>B(OH)2
③氧化性:F>Si>O
④还原性:HCl<H2S<SiH4.
①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Mg(OH)2>B(OH)2
③氧化性:F>Si>O
④还原性:HCl<H2S<SiH4.
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
14.现有三种可溶性物质A、B、C,其中A、B是盐,C是碱,它们溶于水后电离产生的所有离子如下表所示:
回答下列问题:
(1)C的化学式为Ba(OH)2.
(2)A溶液与B溶液反应可生成气体X,则NA个X分子的质量为44,该反应的离子方程式为2H++CO32-=H2O+CO2↑.
(3)A、B溶液分别与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸.
①B的化学式为NaHSO4,鉴别B溶液中溶质电离m的阴离子的试剂为盐酸、BaCl2溶液.
②D溶于稀硝酸的离子方程式为2H++BaCO3=Ba2++H2O+CO2↑.
③D与E的混合物ag,加入足量盐酸,完全反应生成的气体在标准状况下的体积为bL,则E在混合物中的质量分数的表达式为$\frac{a-\frac{197V}{22.4}}{a}$×100%.
| 阳离子 | Na+ | H+ | Ba2+ |
| 阴离子 | OH- | CO32- | SO42- |
(1)C的化学式为Ba(OH)2.
(2)A溶液与B溶液反应可生成气体X,则NA个X分子的质量为44,该反应的离子方程式为2H++CO32-=H2O+CO2↑.
(3)A、B溶液分别与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸.
①B的化学式为NaHSO4,鉴别B溶液中溶质电离m的阴离子的试剂为盐酸、BaCl2溶液.
②D溶于稀硝酸的离子方程式为2H++BaCO3=Ba2++H2O+CO2↑.
③D与E的混合物ag,加入足量盐酸,完全反应生成的气体在标准状况下的体积为bL,则E在混合物中的质量分数的表达式为$\frac{a-\frac{197V}{22.4}}{a}$×100%.
1.DDT是人类合成得到的第一种有机农药,它的结构简式如图所示,有关它的说法正确的是( )
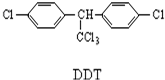

| A. | 它属于芳香烃 | B. | 分子式为C14H8Cl5 | ||
| C. | 1mol该物质能与6mol H2加成 | D. | 分子中最多可能有28个原子共面 |
19.3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成.一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见表:
反应结束后,先分离出甲醇,再加入乙醚进行萃取.
(1)①分离出甲醇的操作是蒸馏.
②萃取用到的分液漏斗使用前需检查是否漏水并洗净,分液时有机层在分液漏斗的上填(“上”或“下”)层.
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤.用饱和NaHCO3 溶液洗涤的目的是除去HCl;用饱和食盐水洗涤的目的是除去少量NaHCO3且减少产物损失.
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是dcab(填字母).
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥.

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃)/g•cm-3 | 溶解性 |
| 甲醇 | 64.7 | / | 0.7915 | 易溶于水 |
| 乙醚 | 34.5 | / | 0.7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 | / | 33-36 | / | 易溶于甲醇、乙醚,微溶于水 |
(1)①分离出甲醇的操作是蒸馏.
②萃取用到的分液漏斗使用前需检查是否漏水并洗净,分液时有机层在分液漏斗的上填(“上”或“下”)层.
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤.用饱和NaHCO3 溶液洗涤的目的是除去HCl;用饱和食盐水洗涤的目的是除去少量NaHCO3且减少产物损失.
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是dcab(填字母).
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥.