题目内容
异丁烯[CH2=C(CH3)2]是重要的化工原料.
已知:
(1)异丁烯和苯酚在一定条件下反应生成对叔丁基酚( ),该反应属于 反应(填“反应类型”).
),该反应属于 反应(填“反应类型”).
(2)对叔丁基酚和甲醛在催化剂作用下可生成油溶性聚合物,写出该反应的化学方程式 .
(3)写出符合下列条件的对叔丁基酚的所有同分异构体的结构简式 .
①含相同官能团;②不属于酚类;③苯环上的一溴代物只有一种.
(4)已知由异丁烯的一种同分异构体A,经过一系列变化可合成物质,其合成路线如图:

①条件1为 ;
②写出结构简式:A ;B .
(5)异丁烯可二聚生成CH2=C(CH3)CH2C(CH3)3,写出该二聚物的名称 .异丁烯二聚时,还会生成其他的二聚烯烃类产物,写出其中一种链状烯烃的结构简式 .
已知:

(1)异丁烯和苯酚在一定条件下反应生成对叔丁基酚(
 ),该反应属于
),该反应属于(2)对叔丁基酚和甲醛在催化剂作用下可生成油溶性聚合物,写出该反应的化学方程式
(3)写出符合下列条件的对叔丁基酚的所有同分异构体的结构简式
①含相同官能团;②不属于酚类;③苯环上的一溴代物只有一种.
(4)已知由异丁烯的一种同分异构体A,经过一系列变化可合成物质,其合成路线如图:

①条件1为
②写出结构简式:A
(5)异丁烯可二聚生成CH2=C(CH3)CH2C(CH3)3,写出该二聚物的名称
考点:有机物的合成,有机物分子中的官能团及其结构
专题:有机物的化学性质及推断
分析:(1)异丁烯和苯酚在一定条件下反应生成对叔丁基酚( ),C=C转化为C-C;
),C=C转化为C-C;
(2)对叔丁基酚和甲醛在催化剂作用下可生成油溶性聚合物,为酚醛缩合反应;
(3)对叔丁基酚的所有同分异构体符合:①含相同官能团-OH;②不属于酚类,-OH与苯环不直接相连;③苯环上的一溴代物只有一种,苯环上只有一种H;
(4)由合成流程可知,最后生成-COOH,则-OH在短C原子上氧化生成-COOH,所以A为CH3CH2CH=CH2,B为CH3CH2CHOHCH2OH;
(5)CH2=C(CH3)CH2C(CH3)3,主链为含C=C的5个C的戊烯,2、4号C上有3个甲基;异丁烯二聚时,生成含1个碳碳双键的有机物.
 ),C=C转化为C-C;
),C=C转化为C-C;(2)对叔丁基酚和甲醛在催化剂作用下可生成油溶性聚合物,为酚醛缩合反应;
(3)对叔丁基酚的所有同分异构体符合:①含相同官能团-OH;②不属于酚类,-OH与苯环不直接相连;③苯环上的一溴代物只有一种,苯环上只有一种H;
(4)由合成流程可知,最后生成-COOH,则-OH在短C原子上氧化生成-COOH,所以A为CH3CH2CH=CH2,B为CH3CH2CHOHCH2OH;
(5)CH2=C(CH3)CH2C(CH3)3,主链为含C=C的5个C的戊烯,2、4号C上有3个甲基;异丁烯二聚时,生成含1个碳碳双键的有机物.
解答:
解:(1)异丁烯和苯酚在一定条件下反应生成对叔丁基酚( ),C=C转化为C-C,则为烯烃的加成反应,故答案为:加成;
),C=C转化为C-C,则为烯烃的加成反应,故答案为:加成;
(2)对叔丁基酚和甲醛在催化剂作用下可生成油溶性聚合物,为酚醛缩合反应,该反应为 ,
,
故答案为: ;
;
(3)对叔丁基酚的所有同分异构体符合:①含相同官能团-OH;②不属于酚类,-OH与苯环不直接相连;③苯环上的一溴代物只有一种,苯环上只有一种H,符合条件的结构简式为 ,故答案为:
,故答案为: ; (
; (
(4)由合成流程可知,最后生成-COOH,则-OH在短C原子上氧化生成-COOH,所以A为CH3CH2CH=CH2,B为CH3CH2CHOHCH2OH,
①由A→B的转化可知,条件1为KMnO4/OH-,故答案为:KMnO4/OH-;
②由上述分析可知,A为CH3CH2CH=CH2,B为CH3CH2CHOHCH2OH,故答案为:CH3CH2CH=CH2;CH3CH2CHOHCH2OH;
(5)CH2=C(CH3)CH2C(CH3)3,主链为含C=C的5个C的戊烯,2、4号C上有3个甲基,名称为2,4,4-三甲基-1-戊烯;异丁烯二聚时,生成含1个碳碳双键的有机物,则还可能生成CH2=C(CH3)CH2CH2CH(CH3)2或(CH3)2C=CHC (CH3)3或(CH3)2C=CHCH2CH(CH3)2,
故答案为:2,4,4-三甲基-1-戊烯;CH2=C(CH3)CH2CH2CH(CH3)2或(CH3)2C=CHC (CH3)3或(CH3)2C=CHCH2CH(CH3)2.
 ),C=C转化为C-C,则为烯烃的加成反应,故答案为:加成;
),C=C转化为C-C,则为烯烃的加成反应,故答案为:加成;(2)对叔丁基酚和甲醛在催化剂作用下可生成油溶性聚合物,为酚醛缩合反应,该反应为
 ,
,故答案为:
 ;
;(3)对叔丁基酚的所有同分异构体符合:①含相同官能团-OH;②不属于酚类,-OH与苯环不直接相连;③苯环上的一溴代物只有一种,苯环上只有一种H,符合条件的结构简式为
 ,故答案为:
,故答案为: ; (
; ((4)由合成流程可知,最后生成-COOH,则-OH在短C原子上氧化生成-COOH,所以A为CH3CH2CH=CH2,B为CH3CH2CHOHCH2OH,
①由A→B的转化可知,条件1为KMnO4/OH-,故答案为:KMnO4/OH-;
②由上述分析可知,A为CH3CH2CH=CH2,B为CH3CH2CHOHCH2OH,故答案为:CH3CH2CH=CH2;CH3CH2CHOHCH2OH;
(5)CH2=C(CH3)CH2C(CH3)3,主链为含C=C的5个C的戊烯,2、4号C上有3个甲基,名称为2,4,4-三甲基-1-戊烯;异丁烯二聚时,生成含1个碳碳双键的有机物,则还可能生成CH2=C(CH3)CH2CH2CH(CH3)2或(CH3)2C=CHC (CH3)3或(CH3)2C=CHCH2CH(CH3)2,
故答案为:2,4,4-三甲基-1-戊烯;CH2=C(CH3)CH2CH2CH(CH3)2或(CH3)2C=CHC (CH3)3或(CH3)2C=CHCH2CH(CH3)2.
点评:本题考查有机物合成及结构与性质,为高考常见题型,把握合成反应中官能团的变化、官能团与性质的关系为解答的关键,(3)中同分异构体推断为解答的难点,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 在新能领域中,氢能已经普遍被认为是一种最理想的新世纪无污染的绿色能,21世纪将是氢能的世纪.电解尿素[CO(NH2)2]的碱性溶液制氢气的装置示意图如图(电解池中隔膜仅阻止气体通过,a、b极均为惰性电极).下列说法正确的是( )
在新能领域中,氢能已经普遍被认为是一种最理想的新世纪无污染的绿色能,21世纪将是氢能的世纪.电解尿素[CO(NH2)2]的碱性溶液制氢气的装置示意图如图(电解池中隔膜仅阻止气体通过,a、b极均为惰性电极).下列说法正确的是( )| A、电解时,b极是阴极放出H2,发生氧化反应 |
| B、溶液中OH-逐渐向b极移动 |
| C、电解时,a极的电极反应式为:CO(NH2)2+8OH-6e-═CO32-+N2↑+6H2O |
| D、若在b极产生标准状况下224mL H2,则消耗尿素2g |
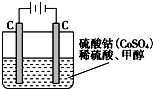
 如图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO43-+2I-+2H+?AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒.甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液.下列叙述中正确的是( )
如图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO43-+2I-+2H+?AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒.甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液.下列叙述中正确的是( )| A、甲组操作时,电流计(G)指针发生偏转 |
| B、甲组操作时,溶液颜色变浅 |
| C、乙组操作时,C2做正极 |
| D、乙组操作时,C1上发生的电极反应为I2+2e-═2I- |
下列操作会使H2O的电离平衡向正方向移动,且所得溶液呈酸性的是( )
| A、向水中加入少量的CH3COONa |
| B、向水中加入少量的NaHSO4 |
| C、向水中加入NaI并加热至100℃,pH=6 |
| D、向水中加少量的KAl(SO4)2 |
从海水中提取镁的工艺流程如图所示.下列说法错误的是( )
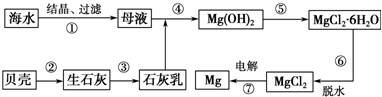

| A、用此法提取镁的优点之一是原料来源丰富 |
| B、步骤⑦电解MgCl2时阴极产生氯气 |
| C、步骤⑥可将晶体置于HCl气氛中脱水 |
| D、上述工艺流程中涉及化合、分解和复分解反应 |
下列有关物质性质的应用正确的是( )
| A、P2O5能与水反应,可用于干燥氨气 |
| B、MgO是一种电解质,工业上常用电解MgO冶镁 |
| C、福尔马林具有防腐杀菌效果,可用于浸制生物标本 |
| D、PbO2具有氧化性和导电性,可用作铅蓄电池负极材料 |
 .
.