题目内容
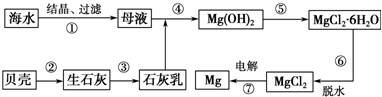
从海水中提取镁的工艺流程如图所示.下列说法错误的是( )

| A、用此法提取镁的优点之一是原料来源丰富 |
| B、步骤⑦电解MgCl2时阴极产生氯气 |
| C、步骤⑥可将晶体置于HCl气氛中脱水 |
| D、上述工艺流程中涉及化合、分解和复分解反应 |
考点:海水资源及其综合利用
专题:元素及其化合物
分析:从海水中提取镁的工艺流程:利用贝壳分解生成氧化钙,溶于水得到氢氧化钙加入到母液中沉淀镁离子,过滤得到氢氧化镁沉淀,加入盐酸溶解富集镁元素,通过浓缩蒸发冷却结晶方法得到氯化镁晶体,氯化氢气流中脱水得到氯化镁固体,电解熔融氯化镁制备镁;
A.从海水中制取镁,原料来源丰富;
B.根据电解时,阴极是阳离子放电;
C.考虑镁离子的水解,一定条件是防止水解的发生;
D.根据从海水中提取镁的工艺流程分析各反应类型.
A.从海水中制取镁,原料来源丰富;
B.根据电解时,阴极是阳离子放电;
C.考虑镁离子的水解,一定条件是防止水解的发生;
D.根据从海水中提取镁的工艺流程分析各反应类型.
解答:
解:从海水中提取镁的工艺流程:利用贝壳分解生成氧化钙CaCO3
CaO+CO2↑,溶于水得到氢氧化钙CaO+H2O═Ca(OH)2,加入到母液中沉淀镁离子Mg2++2OH -=Mg(OH)2↓,过滤得到氢氧化镁沉淀,加入盐酸溶解富集镁元素2HCl+Mg(OH)2═MgCl2+2H2O,通过浓缩蒸发冷却结晶方法得到氯化镁晶体,氯化氢气流中脱水得到氯化镁固体,电解熔融氯化镁制备镁MgCl2
Mg+Cl2↑;
A.海水中镁元素含量高,原料来源于海水,提取镁原料来源丰富,故A正确;
B.电解熔融MgCl2可得到金属镁,镁离子在阴极放电,电极反应方程式为:Mg2++2e-=Mg,故B错误;
C.MgCl2?6H2O在一定条件下加热得到无水MgCl2,若直接加热MgCl2?6H2O,会促进Mg2+水解,得不到无水MgCl2,因Mg2+水解呈酸性,在氯化氢气流中可抑制Mg2+水解,同时带走水蒸气,故一定条件为在HCl气流中,目的是抑制Mg2+水解,故C正确;
D.上述工艺流程中涉及②为分解反应③为化合反应,④为复分解反应,⑤⑥为复分解反应,⑦为分解反应,故D正确;
故选:B.
| ||
| ||
A.海水中镁元素含量高,原料来源于海水,提取镁原料来源丰富,故A正确;
B.电解熔融MgCl2可得到金属镁,镁离子在阴极放电,电极反应方程式为:Mg2++2e-=Mg,故B错误;
C.MgCl2?6H2O在一定条件下加热得到无水MgCl2,若直接加热MgCl2?6H2O,会促进Mg2+水解,得不到无水MgCl2,因Mg2+水解呈酸性,在氯化氢气流中可抑制Mg2+水解,同时带走水蒸气,故一定条件为在HCl气流中,目的是抑制Mg2+水解,故C正确;
D.上述工艺流程中涉及②为分解反应③为化合反应,④为复分解反应,⑤⑥为复分解反应,⑦为分解反应,故D正确;
故选:B.
点评:本题考查元素及其化合物,明确流程中发生的化学反应是解答的关键,注重基础知识和实验基本技能的训练,题目难度中等.

练习册系列答案
相关题目
等体积等物质的量浓度的四种溶液:①(NH4)2SO4溶液②NH4Cl溶液③CH3COONH4溶液④(NH4)2Fe(SO4)2溶液,下列有关四种溶液的说法正确的是( )
| A、常温下,测得③溶液的pH=7,说明该溶液中的CH3COO-与NH4+没有发生水解 |
| B、这四种溶液中c(NH4+)大小顺序为:④>①>③>② |
| C、向②溶液中加一定量的浓氨水,可能会出现:c(NH4+)═c(Cl-) |
| D、向盛有少量苯酚溶液的试管中滴加几滴④溶液,可以看到溶液呈紫色 |
向NaOH(aq)滴入HCOOH(aq)的过程中,所得到的混合溶液中离子浓度的大小关系可能正确的是( )
| A、c(OH-)=c(Na+)>c(HCOO-)>c(H+) |
| B、c(Na+)=c(HCOO-) |
| C、c(Na+)>c(HCOO-)>c(OH-)>c(H+) |
| D、c(H+)>c(HCOO-)>c(Na+)>c(OH-) |
某有机物的分子式为C9H9ClO2,分子中含有1个苯环,苯环上有两个取代基,并能与NaHCO3溶液反应的同分异构体的数目为(不考虑立体异构)( )
| A、12种 | B、15种 |
| C、18种 | D、21种 |
有三种不同的基团,分别为-X、-Y、-Z,若同时分别取代苯环上的三个氢原子,能生成的同分异构体数目是( )
| A、10种 | B、8种 | C、6种 | D、4种 |

 ),该反应属于
),该反应属于
 )的废水可以利用微生物电池除去,其原理如图1所示.
)的废水可以利用微生物电池除去,其原理如图1所示.